1、选择题 有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6,其发烟过程中的化学反应为:①3ZnO+2Al═Al2O3+3Zn?②3Zn+C2Cl6═3ZnCl2+2C
下列有关叙述不正确的是( )
A.反应①是铝热反应
B.反应②是置换反应
C.烟幕是小液滴分散在空气中形成的
D.C2Cl6属于卤代烃
参考答案:A、反应①是Al与ZnO发生置换反应,属于铝热反应,故A正确;?
B、反应②是Zn与化合物C2Cl6反应生成化合物ZnCl2与单质C,符合置换反应概念,属于置换反应,故B正确;
C、由反应方程式可知,生成物都是固体,是固体小颗粒分散在空气中形成的烟幕,不是小液滴,故C错误;
D、C2Cl6是乙烷的完全取代产物,属于卤代烃,故D正确;
故选C.
本题解析:
本题难度:一般
2、计算题 (6分)2005年国家质检总局铝合金抽检合格率约为90%。已知国家行业标准中铸造铝合金的各成分的质量分数为:Si—4.5%—5.5%,Cu—1.0%—1.5%,Mg—0.4%—0.6%,其余为Al。
现对某品牌的铸造铝合金中所含的四种成分作如下的实验检测:
①称取18.0 g铸造铝合金样品,分成等质量的A、B两份。向A份加入足量NaOH溶液,B份加入足量的稀盐酸。(已知:Si+2NaOH+H2O====Na2SiO3+2H2↑)
②待两份反应物都充分反应之后,称得滤渣质量相差0.512 g,收集得到的两份气体的体积相差851.2 mL(标准状况下)。
试完成下列问题:
(1)样品中Si和Mg的物质的量分别是多少?
(2)通过计算判断该品牌的铸造铝合金是否为合格产品。
参考答案:(1)0.02 mol? 0.002 mol
(2)不合格产品
本题解析:(1)设9 g样品中所含Si的物质的量为x,Mg的物质的量为y。
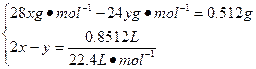
解得:x="0.02" mol,y="0.002" mol
(2)因为合金中Si的百分含量为:0.02 mol×28 g·mol-1÷9 g×100%=6.2%,超过国家标准,故该铸造铝合金属于不合格产品。
本题难度:一般
3、选择题 下列金属中,能与氢氧化钠溶液反应的是( )
A.铝
B.镁
C.铁
D.铜
参考答案:只有Al与NaOH溶液反应生成偏铝酸钠和氢气,而Mg、Fe、Cu均不与NaOH溶液反应,
故选A.
本题解析:
本题难度:一般
4、选择题 下列实验描述,符合事实的是
[? ]
A.金属钠暴露在空气中,表面变暗,生成白色固体氧化钠
B.用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的白光,放出大量的热,产生白色固体
C.用坩埚钳夹住铝箔在酒精灯上点燃,发出耀眼的白光,放出大量的热
D.用坩埚钳夹住铝箔在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落下来
参考答案:AB
本题解析:
本题难度:简单
5、选择题 除去镁粉中的少量铝粉,可选用的试剂是( ? )
A.稀盐酸
B.氨水
C.NaOH溶液
D.氯化钠溶液
参考答案:C
本题解析:
本题难度:一般