1、选择题 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。

则原溶液中Al3+、Mg2+、NH4+的物质的量分别为 ( ?)
A.2 mol、3 mol、8 mol
B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol
D.3 mol、2 mol、4 mol
参考答案:C
本题解析:
加入8molNa2O2时,根据钠原子守恒,可知n(Na+)=2n(Na2O2)=2×8mol=16mol,Na+离子所带的总电量相当于16mol×1=16mol.
A、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2+8mol×1=20mol,故A错误;
B、Al3+、Mg2+、NH4+离子所带的总电量相当于3mol×3+2mol×2+8mol×1=21mol,故B错误;
C、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2+4mol×1=16mol,故C正确;
D、Al3+、Mg2+、NH4+离子所带的总电量相当于3mol×3+2mol×2+4mol×1=17mol,故D错误.
故选C.
本题难度:困难
2、填空题 (6分)已知蓝铜矿的主要成分是2CuCO3・Cu(OH)2,受热易分解。铝土矿的主要成分是Al2O3、Fe2O3、SiO2。经过一定条件的转化二者均可转化为金属单质,根据下列框图转化回答问题:
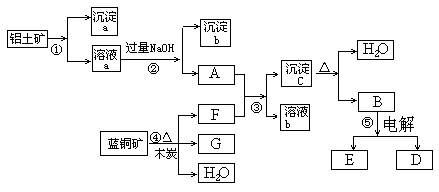
(1)写出①的离子方程式:______________________、_____________________。
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
______________?_______、___________?___________。
(3)若过量F与A反应,溶液b的成分是:__?____(写化学式)。
参考答案:
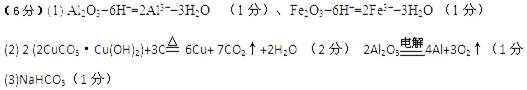
本题解析:略
本题难度:简单
3、填空题 (16分 )镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015?t。从海水中(主要含含Na+,Cl―,Mg2+等离子)提取镁的工艺流程图如下:
)镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015?t。从海水中(主要含含Na+,Cl―,Mg2+等离子)提取镁的工艺流程图如下:
(1)A物质的化学式为?。操作1的名称为?。
(2)试写出向固体A中加入足量盐酸的离子方程式?。
(3)该反应的副产物主要有?等。
(4)若开始得到的固体A的质量为116g,不考虑物质的损失,则最后生成的Mg的物质的量为?mol。
参考答案:
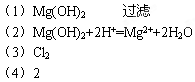
本题解析:略
本题难度:一般
4、选择题 将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是
A.硫酸
B.硝酸钠
C.硫酸锌
D.氯化铜
参考答案:B
本题解析:分析:将铁屑溶于过量的盐酸中,所以说氢离子过量,铁反应完全后,氢离子还有剩余.
A.硫酸不能氧化二价铁离子;
B.硝酸具有强氧化性,可以将二价铁离子氧化为三价铁离子;
C.硫酸锌与二价铁离子不反应;
D.氯化铜与二价铁离子不反应;
解答:盐酸不能把铁氧化到最高价态,将铁屑溶于过量的盐酸中,发生反应:Fe+2HCl=FeCl2+H2↑
A.因为盐酸硫酸不具备强氧化性,不能氧化二价铁离子,所以,没有三价铁离子生成,故A错误;
B.将铁加入过量的盐酸中,铁反应完全后氢离子还有剩余,加入硝酸锌后,硝酸锌溶解,电离出硝酸根离子,而硝酸根离子和氢离子在同一溶液相当于硝酸,而硝酸具有强氧化性,可以将二价铁氧化为三价铁离子,故B正确;?
C.硫酸锌溶解,电离出硫酸根离子,与过量的氢离子在同一溶液,相当于稀硫酸,而稀盐酸硫酸不具备强氧化性,不能氧化二价铁离子,故C错误;
D.氯化铜溶于水,电离出氯离子,与过量的氢离子在同一溶液,相当于稀盐酸,盐酸不能把二价铁离子氧化,故D错误;故选B.
点评:该题主要考查了硝酸的氧化性,解题时须注意,题干和选项不一定明显显示加硝酸,通过先后加入的物质形成硝酸溶液.
本题难度:简单
5、选择题 某氧化物不溶于水,溶于NaOH溶液中,生成易溶于水的化合物,向稀盐酸中滴入该溶液,有白色沉淀生成,则原氧化物是(?)
A.Al(OH)3
B.MgO
C.Fe2O3
D.Al2O3
参考答案:D
本题解析:略
本题难度:简单