1、选择题 由碳、氧两种元素组成的气体中,碳与氧的质量比为3∶5,则该气体可能是(?)
A.由CO或CO2单独组成的纯净物
B.由CO和CO2共同组成的混合物
C.由CO和O2共同组成的混合物
D.由CO2和O2共同组成的混合物
参考答案:BC
本题解析:由碳、氧元素组成的纯净物有CO和CO2,CO中碳、氧元素质量比是3∶4,CO2中碳、氧元素质量比为3∶8,因此不可能是CO或CO2中的一种组成,A错误;选项B,CO与CO2组成的混合气体,碳、氧元素质量比肯定小于3∶4而大于3∶8,有可能是3∶5,正确;选项C,CO与O2的混合物,碳、氧元素质量比小于3∶4而大于3∶8,有可能是3∶5,正确;选项D,碳、氧元素质量比会小于3∶8,不可能是3∶5,错误。
本题难度:简单
2、选择题 对CO2和SiO2来说,正确的是(?)
A.都是直接由分子构成的
B.固体的晶体类型相同
C.物理性质基本一致
D.都是酸性氧化物,均能与碱反应生成盐和水
参考答案:D
本题解析:CO2(干冰)是分子晶体,SiO2为原子晶体,两者物理性质差异很大,但是都是酸性氧化物,均能与碱反应生成盐和水。故选D项。
本题难度:简单
3、选择题 在密闭容器中,盛有4 g O2和4 g C,加热使之充分反应后得到的气体是(?)
A.CO
B.CO2
C.CO和CO2
D.O2和CO2
参考答案:A
本题解析:n(O2)=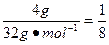 mol,n(C)=
mol,n(C)=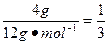 ?mol。
?mol。
C+O2====CO2,2C+O2====2CO
若只生成CO2需C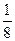 ?mol,若只生成CO需C
?mol,若只生成CO需C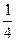 ?mol。
?mol。
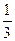 ?mol>
?mol>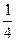 mol>
mol>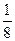 mol,即全部生成CO,C仍过量。
mol,即全部生成CO,C仍过量。
本题难度:简单
4、选择题 下列各组中的两种物质作用时,反应条件(温度、反应物用量)改变,不会引起产物种类改变的是
[? ]
A.Na和O2
B.NaOH和CO2
C.Na2O2和CO2
D.C 和O2
参考答案:C
本题解析:
本题难度:简单
5、填空题 硅及其化合物对人类现代文明具有特殊贡献,请回答下列有关问题:
(1)硅原子的结构示意图:________。
(2)下列物品或设备所用的材料属于硅酸盐的是________。
①长江三峡水泥大坝;②石英光导纤维;③陶瓷坩埚;④普通玻璃;⑤硅太阳能电池
A.①②③?B.③④⑤? C.②③④?D.①③④
(3)常温下,SiCl4为液态,沸点为57.6℃,在空气中冒白雾。制备高纯度硅的中间产物SiCl4中溶有液态杂质,若要得到高纯度SiCl4,应采用的方法是________;用化学方程式及必要文字解释SiCl4在空气中冒白雾的原因:_______________________________________。
(4)工业上可用SiCl4(g)制备高温结构陶瓷氮化硅,其反应方程式为
3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)
Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)
①该反应的平衡常数表达式K=______________.
②在密闭恒容容器中,能表示上述反应达到平衡状态的是________。
A.3v逆(N2)=v正(H2)
B.v正(HCl=4v正=4v正(SiCl4)
C.混合气体密度保持不变
D.c(N2)∶c(H2)∶c(HCl)=1∶3∶6
③在某条件下达到平衡时,H2与HCl物质的量之比为m∶n;保持其他条件不变,降低温度达到平衡时,H2与HCl物质的量之比________m∶n(填“>”、“=”或“<”)。
参考答案:(1)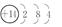
(2)D
(3)干燥条件下蒸馏 SiCl4+3H2O=H2SiO3+4HCl,HCl遇水蒸气产生白雾
(4)①K=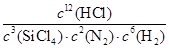 ②AC ③<
②AC ③<
本题解析:(1)硅原子的原子核内含14个质子,原子核外有3个电子层,每个电子层上的电子数分别为2个、8个和4个,所以其原子结构示意图为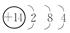 。(2)长江三峡大坝的水泥中含有硅酸盐,石英光导纤维的主要成分是SiO2,不是硅酸盐,陶瓷坩埚中含有硅酸盐,玻璃中含有硅酸盐,硅太阳能电池中含有单质硅的成分,不含硅酸盐。(3)由SiCl4的沸点低的性质可以选择蒸馏的方法纯化,但因为SiCl4能够水解,所以必须选择无水(无水蒸气)的环境进行该操作;SiCl4在空气中与水蒸气反应生成H2SiO3和HCl,其中HCl在空气中遇到水蒸气产生白雾。(4)①因氮化硅是固体,所以该反应的平衡常数为K=
。(2)长江三峡大坝的水泥中含有硅酸盐,石英光导纤维的主要成分是SiO2,不是硅酸盐,陶瓷坩埚中含有硅酸盐,玻璃中含有硅酸盐,硅太阳能电池中含有单质硅的成分,不含硅酸盐。(3)由SiCl4的沸点低的性质可以选择蒸馏的方法纯化,但因为SiCl4能够水解,所以必须选择无水(无水蒸气)的环境进行该操作;SiCl4在空气中与水蒸气反应生成H2SiO3和HCl,其中HCl在空气中遇到水蒸气产生白雾。(4)①因氮化硅是固体,所以该反应的平衡常数为K=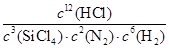 。②同一个化学反应中,用不同物质表示的化学反应速率大小与其计量系数成正比,选项A给出了正反应速率与逆反应速率的关系,A项正确;选项B给出的是不同种物质的正反应速率的关系,其关系在没有达到平衡的时候也存在,B项错;选项C,密闭容器的容积不变,而根据化学方程式可知,在达到平衡前,由于生成固体氮化硅,故容器内混合气体的质量减小,所以密度减小,当达到平衡时,各物质的生成与消耗相等,混合气体的质量不再变化,密度恒定,C项正确;可逆反应进行的限度与化学方程式中的计量系数之间没有联系,D项错。③由给出的反应方程式中的ΔH= a kJ/mol(a<0)可知,该反应为放热反应,降低温度平衡向正反应方向移动,所以H2与HCl的物质的量之比变小。
。②同一个化学反应中,用不同物质表示的化学反应速率大小与其计量系数成正比,选项A给出了正反应速率与逆反应速率的关系,A项正确;选项B给出的是不同种物质的正反应速率的关系,其关系在没有达到平衡的时候也存在,B项错;选项C,密闭容器的容积不变,而根据化学方程式可知,在达到平衡前,由于生成固体氮化硅,故容器内混合气体的质量减小,所以密度减小,当达到平衡时,各物质的生成与消耗相等,混合气体的质量不再变化,密度恒定,C项正确;可逆反应进行的限度与化学方程式中的计量系数之间没有联系,D项错。③由给出的反应方程式中的ΔH= a kJ/mol(a<0)可知,该反应为放热反应,降低温度平衡向正反应方向移动,所以H2与HCl的物质的量之比变小。
本题难度:一般