1、实验题 (8分)现使用酸碱中和滴定法测定市售白醋的总酸量(g/100 mL)。
Ⅰ.实验步骤:
(1)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到100 mL________(填仪?器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴________作指示剂。
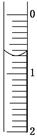
(3)读取盛装0.100 0 mol/L NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________ mL。
(4)滴定。当____________________?________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录:
滴定次数
实验数据(mL)
| 1
| 2
| 3
| 4
|
V(样品)
| 20.00
| 20.00
| 20.00
| 20.00
|
V(NaOH)(消耗)
| 15.95
| 15.00
| 15.05
| 14.95
|
?
Ⅲ.实验处理:
(1)某同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=(15.95+15.00+15.05+14.95)/4 mL=15.24 mL。
指出他的计算的不合理之处:____________? _? _。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是(填写序号)________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
参考答案:Ⅰ.(1)容量瓶 (2)酚酞 (3)0.70 (4)溶液由无色恰好变为红色,并在半分钟内不褪色
Ⅲ.(1)第1次滴定误差明显大,属异常值,应舍去 0.75 4.5 (2)c (3)ab
本题解析:依据中和滴定原理,确定所需仪器、药品、实验步骤,关注每步操作要领及意义。
Ⅰ(1)定容一般要在容量瓶中进行,所以转移到100 mL容量瓶中定容。
(2)强碱与弱酸的滴定,生成的是强碱弱酸盐,显碱性,最好选碱性范围内变色的指示剂,此处指示剂是酚酞。
(3)注意读数从上到下依次递增,此处为0.70mL;
(4)当溶液由无色恰好变为红色,并在半分钟内不褪色时,停止滴定。
Ⅲ. (1)很明显第一组数据比其余三组数据偏大,不能选用,要舍去。
(2)碱式滴定管在滴定时未用标准NaOH溶液润洗,导致标准液浓度偏低,使用时体积偏大,则导致待测液浓度偏大;碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,会导致测定的标准液体积偏大,待测液的浓度偏大;锥形瓶中加入待测白醋溶液后,再加少量水,并不影响结果;锥形瓶在滴定时剧烈摇动,有少量液体溅出,使用的标准液减少,则待测液浓度偏小。
点评:计算平均值时,一定要注意误差较大的数据要舍去。本题难度不大,较综合。
本题难度:一般
2、填空题 (共15分)下图是实验室制取溴苯的装置。填写以下内容:
(1)写出反应的化学方程式?
(2)导管a段的作用?。导管b段末端跟锥形瓶里液面保持一段距离的目的是____________________,若锥形瓶内盛硝酸银溶液,图中虚线方框部分的作用
?。
(3)反应后不久导管b出口可见到什么现象?。
若锥形瓶内盛硝酸银溶液,反应后出现淡黄色,______(填“能”或“不能”)证明苯与溴单质发生取代反应,这是因为___________________________________
(4)反应得到的溴苯呈______色,这是因为??;为除去混入溴苯中的溴,可加入_____________试剂,用?方法分离。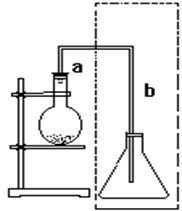
参考答案:(1)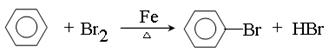
(2)导气 防倒吸 检验溴离子 (3)白雾 能 说明溴离子产生
(4)黄 溶有一定溴 氢氧化钠 分液
本题解析:(1)在催化剂的作用下,苯和液溴发生取代反应生成溴苯。
(2)因为生成物溴化氢是气体,所以通过导管把溴化氢导入到锥形瓶中。溴化氢极易溶于水,所以为了防止倒吸导管b段末端跟锥形瓶里液面保持一段距离。硝酸银和溴离子反应生成浅黄色溴化银沉淀,原来检验溴离子。
(3)溴化氢极易和水蒸气结合,形成白雾。根据沉淀颜色证明锥形瓶内含有溴离子,因此可以说明反应是取代反应。
(4)溴苯由于溶解类溴而显黄色,因为溴苯难溶于水,所以可以通过氢氧化钠除去单质溴,然后分液即可。
本题难度:一般
3、填空题 实验室常用消石灰和NH4Cl固体混合加热制取氨气,回答下列问题:
(1)写出该反应的化学方程式?。
(2)要得到纯净干燥的氨气,可选用的干燥剂是?。
A.浓硫酸
B.碱石灰
C.五氧化二磷
D.固体NaOH