1、选择题 用酚酞作指示剂,以0.100 mol・L-1的NaOH溶液测定装在锥形瓶中的一定体积的盐酸溶液的物质的量浓度。下列操作将导致测定值高于实际值的是
[? ]
A.标准液在0刻度线以上,未予调整就开始滴定
B.碱式滴定管用蒸馏水洗涤后未用标准NaOH溶液润洗
C.观察记录滴定管内液面刻度时滴定前仰视,滴定后俯视?
D.酚酞指示剂由无色变为红色时立即停止滴定
2、实验题 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验。
请完成下列填空:
①配制100mL 0.10mol/L NaOH标准溶液。
②取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3 次,记录数据如下。
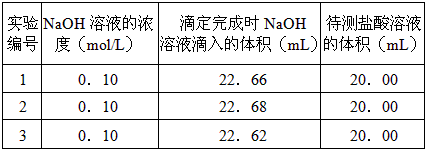
(1)碱式滴定管用蒸馏水洗净后在装碱液之前,还应该进行的操作是:_______________________。
(2)滴定达到终点的现象是______________________。
(3)根据上述数据,可计算出该盐酸的浓度约为______________。(保留两位有效数字)
(4)除去碱式滴定管中气泡的方法应采用操作______________________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。(填序号)

(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有__________。(多选扣分)
A.滴定前平视读书,终点读数时仰视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后又用标准盐酸润洗
D.称量前NaOH固体中混有Na2CO3固体
E.配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F.碱式滴定管尖嘴部分有气泡,滴定后消失
3、填空题 I.如图1为向25mL 0.1mol・L-1NaOH溶液中逐滴滴加0.2mol・L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答
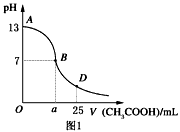
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?
________(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?
________区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项________(选填字母)。

(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)大于c(CH3COO-)
B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)
D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)________2c(Na+)(填“>”“<”或“=”)。
Ⅱ.t℃时,某稀硫酸溶液中c(H+) =10-amol・L-1,c(OH-) =10-bmol・L-1,已知a+b=13
(5)该温度下水的离子积常数Kw的数值为________。
(6)该温度下(t℃),将100mL 0.1mol・L-1的稀H2SO4与100mL 0.4mol・L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。
4、实验题 某学生用物质的量的浓度为amol/L的标准NaOH去测定VmL HCl溶液的物质的量浓度。回答下列问题: (1)实验前应先检查滴定管__________________,实验过程中眼睛__________________;
(2)其操作可分解为如下几步:
A.取V/4 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液;
B.用标准氢氧化钠溶液润洗滴定管2~3次;
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2~3mL处;
E.调节液面至“0”至“0”刻度以下,记下读数;
F.把锥形瓶放在滴定管的下面,用标准氢氧化钠溶液滴定至终点并主下滴定管的读数;
正确的操作顺序是:___ 、D 、 _____ 、 _____、 A、____ ;
(3)滴定至终点时的现象是:_____________________
(4)下图是碱式滴定管中液面在滴定前后的读数
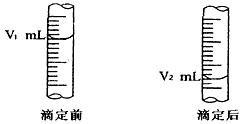
c (HCl) =__________________
(5)下列操作会使测定的HCl物质的量浓度偏大的是________________
A、滴定前碱式滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失;
B、滴定终点后溶液颜色迅速消失;
C、滴定前仰视,滴定终了平视;
D、实验前先用待测液润洗锥形瓶;
E、碱式滴定管用蒸馏水洗净后,未用标准溶液润洗,使滴定结果;
5、选择题 下列实验操作会引起测量结果偏高的是
[? ]
①用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡。
②配制烧碱溶液时,将称量后的NaOH固体溶于水,立即移入容量瓶,将洗涤烧杯的液体注入容量瓶后,加蒸馏水至刻度线。
③中和滴定时,锥形瓶内有少量水。
④用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,酸式滴定管用蒸馏水洗涤后,未用标准液润洗。
⑤用已知液滴定未知液时,读取滴定管终点读数时,俯视刻度线。
A.只有④
B.只有②④
C.只有②④⑤
D.全部