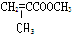|
�߿���ѧ���⡶��ɫ��ѧ�����㹮�̣�2019�����°棩(��)
2019-06-28 22:37:09
�� �� �� ��
|
1��ʵ���� [��ѧ����ѡ��ѧ�뼼��]��15�֣�
�����ǹ�ҵ��������Ϊ��Ҫ�IJ�Ʒ֮һ��
��1����ҵ����������Ҫ��Ϊ_________��________��_________�����Ρ�
��2�������ǵڶ��η�Ӧ���й�ʵ�����ݣ���ѡ������ʵ���������____________��
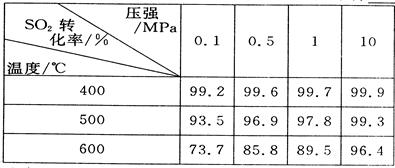
��3����������߷�Ӧ���ʺ�SO2��ת���ʣ����д�ʩ���е��ǣ�?��
A����װ����ͨ�뵪���ұ����������
B����װ����ͨ�������ұ����������
C�����Ӹ���Ĵ���
D�������¶ȣ���ʱת��SO3
| ��4������������β���к�������SO2������ʯ��ˮ���պ��������ᴦ�����˹����漰�Ļ�ѧ��Ӧ����ʽΪ__________________��______________��
��5��������ڶ��������豸��������������Ϊ��SO27%��O211%��N282%������100��������Ļ�������ڷ�Ӧ����96.7�������Ӧ����������N2��SO3�������Ϊ___________����ʱSO2ת����Ϊ__________��
�ο��𰸣���1������?�Ӵ�����?���գ���1�֣�
��2��400? 0.4Mpa?����ѹ������1�֣�?��3��B��2�֣�
��4��SO2+Ca��OH��2=CaSO3+H2O? CaSO3+H2SO4=CaSO4+SO2+H2O
��5��410:33����82��6.6��? 94.3%����2�֣�
���������(1)���鹤ҵ�������ԭ������ҵ����������Ҫ��Ϊ�������Ӵ����������������Ρ�
��2�����ݱ������ݿ�֪���¶�Խ��ת����Խ�ͣ������ۺϿ����¶ȶԷ�Ӧ���ʡ���ѧƽ�⼰�����Ļ��Եȣ�ѡ��400�档ѹǿԽ��ת����Խ�ߣ���ѹǿ̫�ߣ����豸��Ҫ����ߣ����ٳ�ѹ�·�Ӧ���ת�����Ѿ��ܸߣ����Բ��ó�ѹ���ɡ�
��3��A�з�Ӧ���Ũ�Ȳ��䣬��Ӧ���ʺ�ת���ʶ����䡣����������Ũ�ȣ���Ӧ��������ƽ��������Ӧ�����ƶ���ת��������B��ȷ������ֻ�ܸı䷴Ӧ���ʣ�������Ӱ��ƽ��״̬��C����ȷ�������¶ȷ�Ӧ���ʽ��ͣ�D����ȷ����ѡB��
��4��SO2������������ܺ�ʯ��ˮ��Ӧ������������ơ�������ƺ����ᷴӦ�ֲ���SO2���йط���ʽΪSO2+Ca��OH��2=CaSO3+H2O��CaSO3+H2SO4=CaSO4+SO2+H2O��
��5��������ݷ���ʽ���йؼ��㣬��Ӧ�ķ���ʽΪ
2SO2��O2 2SO3?��V 2SO3?��V
2? 1? 2? 1
6.6? 3.3? 6.6? 100��96.7��3.3
���Է�Ӧ����������N2��SO3�������Ϊ82�U6.6
SO2��ת������6.6��7��100����94.3%��
�����Ѷȣ�һ��
2��ѡ���� �ӻ�ѧ�Ƕȷ�����������������ȷ����
[? ]
A������̫��������ˮ�Ǻ�ˮ�����ķ���֮һ
B�����ع��ͻ����ټӹ�Ϊʳ���ͣ��Լ���ˮ�帻Ӫ����?
C�����ƿ���ȼ�ϵ�����������ͻ�����β����Ⱦ�����Լ���PM2.5��Ⱦ
D����ɫ��ѧ�ĺ��������û�ѧԭ����Դͷ�ϼ��ٺ�������ũҵ�����ȶԻ�������Ⱦ
�ο��𰸣�B
���������
�����Ѷȣ���
3������� ����ɫ��ѧ������Ҫ����֮һ��ָ�Ӽ�������������ƿ��еĻ�ѧ��Ӧ��ʹԭ�ӳ�����ã���������Ⱦ����л�ѧ��Ӧ���ϡ���ɫ��ѧ��������ǣ�������
A����CuSO4��Cu+2H2SO4��Ũ�� CuSO4+SO2��+2H2O
B����Cu��NO3��2��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O
C�����л������ĵ��壺CH3C��CH+CO+CH3OH
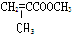
D��

�ο��𰸣�A�����ж���������������ɣ���A����
B�����ж���������������ɣ���B����
C��ԭ��������Ϊ100%����C��ȷ��
D��HBr�Ǹ���Ʒ��ԭ�������ʲ��ߣ���D����
��ѡC��
���������
�����Ѷȣ�һ��
4��ѡ���� �ո���Ŀǰʹ����㷺���ʣ�����Ҫ�ɷ��ǣ�?��
A��Ca5(PO4)3F
B��Ca(H2PO4)2��H2O��CaSO4
C��Ca3(PO4)2��CaHPO4
D��CaHPO4��Ca(H2PO4)2
�ο��𰸣�B
��������������ǻ�ѧ��ʶ�⣬A�������������Ҫ�ɷ֣�B�����ոƵ���Ҫ�ɷ֣�C��D�����������εĻ���û�о��������Ҳû�о������;��
�����Ѷȣ�һ��
5��ѡ���� ���б仯�У����������仯���ǣ�?����
��ʯ�͵ķ���ú�ĸ���?��ʯ�͵��ѻ��������ȷ�Ӧ������ϩ��Ϊ����ϩ����
������ת��Ϊ��������ϩ�����ʵ���౽����ˮ?�ảˮ������ȡ��ˮ
A���٢ڢۢ�
B���٢ڢݢ�
C���٢��
D���٢ڢޢ�
�ο��𰸣�C
��������������������ɵ��ǻ�ѧ�仯����֮�������仯�����Ԣ٢���������仯������ǻ�ѧ�仯����ѡC��
�����Ѷȣ���
|