1、选择题 某氨水的pH=a,某盐酸的pH=b,已知a+b=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是
A.c(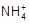 )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
B.c(Cl-)>c(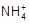 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C.c(Cl-)>c(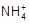 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c(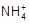 )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)
参考答案:D
本题解析:氨水和盐酸发生中和反应生成氯化铵和水,则根据电荷守恒可知c(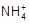 )+c(H+)=c(Cl-)+c(OH-),所以选项D正确,AB不正确;由于氨水是弱碱,且a+b=14,所以在反应中氨水是过量的,溶液显碱性,应该是c(
)+c(H+)=c(Cl-)+c(OH-),所以选项D正确,AB不正确;由于氨水是弱碱,且a+b=14,所以在反应中氨水是过量的,溶液显碱性,应该是c(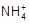 )>c(Cl-)>c(OH-)>c(H+),C不正确,答案选D。
)>c(Cl-)>c(OH-)>c(H+),C不正确,答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确酸碱中和后溶液酸碱性的判断,首先要判断酸碱的过量问题。只有当酸碱恰好反应时,才能考虑生成的盐是否水解,其次要利用好电荷守恒、物料守恒以及质子守恒。
本题难度:一般
2、选择题 常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是(?)
A.a不可能显酸性
B.b不可能显中性
C.a可能显酸性或碱性
D.b可能显碱性或者酸性
参考答案:C
本题解析:由于不知道酸的酸性强弱程度,所以与氨水混合后酸碱性不定。与氢氧化钠溶液混合后,可能为中性(强酸)或酸性(弱酸)。故答案为C
本题难度:一般
3、选择题 常温下,在一定体积pH=12的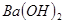 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的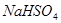 溶液,当溶液中的
溶液,当溶液中的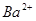 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液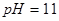 。若反应后溶液的体积等于
。若反应后溶液的体积等于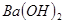 溶液与
溶液与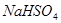 溶液的体积之和,则
溶液的体积之和,则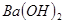 溶液与
溶液与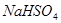 溶液的体积比是
溶液的体积比是
A.1:9
B.1:1
C.1:2
D.1:4
参考答案:D
本题解析:Ba(OH)2和NaHSO4,1:1反应,恰好沉淀完全。此时n(Ba2+)=n(SO)=n(H+)。设Ba(OH)2为V1L、NaHSO4为V2L,有c(OH-)=10-3=,解得,V1:V2=1:4。
本题难度:一般
4、选择题 形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.在农村推广使用沼气
D.减少资源消耗、增加资源的重复使用和资源的循环再生