1、选择题 下列物质既能跟浓H2SO4反应,又能与烧碱反应的是
①MgCl2?②NaHCO3?③(NH4)2 S ?④Al(OH)3
A.只有④
B.除①外
C.除①③
D.全部都可以
参考答案:D
本题解析:氯化镁和浓硫酸反应可以制备氯化氢,另外氯化镁与和烧碱反应生成氢氧化镁白色沉淀。同样分析可知,其余选项都能和浓硫酸以及烧碱反应,答案选D。
点评:该题是中等难度的试题,也是高考中的重要考点。试题综合性强,侧重对基础性知识的巩固与检验,难度不大。该题的关键是记住常见物质的化学性质,然后灵活运用即可。
本题难度:简单
2、推断题 Q、X、Y、Z、W是元素周期表前四周期中的五种常见元素,其相关信息如下表

(1)Y位于元素周期表第___周期第___族,Y和Z的最高价氧化物对应的水化物的酸性较强的是_______ (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在______个σ键。在H-Y、H-Z两种共价键中,键的极性较强的是_______,键长较长的是________。
(3)W的基态原子核外电子排布式是____________,在W的晶体结构中,中心原子的配位数是______。
(4)Q、X形成的最简单化合物里中心原子的杂化类型是________,其空间结构为_________,Q与氧原子形成的化合物中中心原子杂化类型与上述物质相同,但键角不同,其原因可能是____________。
(5)写出与YO2互为等电子体的一种单质的分子式:__________。
参考答案:(1)三;ⅥA;HClO4-
(2)2;H-Cl;H-S
(3)1s22s22p63s23p63d104s1或[Ar]3d104s1;12
(4)sp3;正四面体形;水分子中有两对孤对电子占据两个sp3杂化轨道,使两个氧氢键夹角减小
(5)O3
本题解析:
本题难度:一般
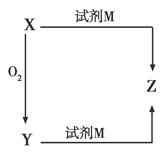
3、选择题 物质X、Y、Z均含有同一种元素,其转化关系如图所示。下列物质X和试剂M的组合不可能是(?)
?
| A
| B
| C
| D
|
X的化学式
| Na2O
| Al
| Mg
| SO2
|
试剂M
| 水
| NaOH溶液
| 稀硫酸
| NaOH溶液
|
?
参考答案:D
本题解析:A组Na2O→Na2O2→NaOH。B组Al→Al2O3→NaAlO2。C组Mg→MgO→MgSO4。D组SO2→Na2SO3或NaHSO3,SO2→SO3→Na2SO4。
本题难度:一般
4、选择题 X、Y、Z、W四种主族元素,若X的阳离子与Y的阴离子具有相同的电子层结构;W的阳离子的氧化性强于等电荷数的X阳离子的氧化性;Z的阴离子半径大于等电荷数的Y的阴离子半径,则四种元素的原子序数由大到小的顺序是
[? ]
A. ZXYW
B. WXYZ
C. XYZW
D. ZYXW
参考答案:B
本题解析:
本题难度:一般
5、选择题 将甲、乙两种非金属的性质相比较,知道
①甲比乙容易与H2化合
②甲原子能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强
④与某金属反应时甲原子得电子数目比乙的多
⑤甲的单质熔、沸点比乙低能说明甲比乙的非金属性强的是
A.①④
B.③⑤
C.①②③
D.①②③④⑤
参考答案:C
本题解析:非金属性强弱的比较主要从以下几方面进行判断:(1)元素周期律,(2)最高价化合物对应的水化物的酸性来判断,(3)其氢化物的稳定性及化合条件,(4)与盐酸之间的置换反应或物质之间的置换反应,(5)反应的条件、剧烈程度和化合物的价态等等.C项正确.
本题难度:一般