1��ѡ���� NA���������ӵ�����������˵����ȷ����
A����״���£�22.4LCH4�к��е�����ĿΪ8NA
B��14gCnH2n�к��е�̼ԭ����ĿΪNA
C��18 g D2O�к��е�������ĿΪ10NA
D��1 L0.5mol/LAlCl3��Һ�к��е�Al3+��ĿΪ0.5NA
�ο��𰸣�B
���������A ����״���£�22.4LCH4�к��е�����ĿΪ10NA
B ��ȷ��14gCnH2n�����ʵ���Ϊ14/n mol,���е�̼ԭ����ĿΪNA
C ����18 g D2O����1mol����1molD2O�к��е�������Ŀ����10NA
D ��������Al3+ˮ�⣬���е�Al3+��ĿС��0.5NA
�����Ѷȣ�һ��
2������� ��ͨ����һ�ֵ���ɫ���壬���������г�ɫ����ɫ������ɫ���֣����Ƕ�����ĵ��ʣ�����ÿ����������ԭ�ӵĸ�����ͬ������SX��ʾ�������������ⶨ�Ľ���ǣ�
��1����ɫ�������ܶ�����ɱ�״������11.34��/�������ķ���ʽΪ��______��
��2������ɫ��������������ͬ״����ͬ���������6.62���������ķ���ʽΪ��______��
��3����ɫ�������ܶ���ͬ״���������ܶȵ�64���������ķ���ʽΪ��______��
�ο��𰸣���1����״���ܶ�Ϊ11.34��/������SX������Ħ������Ϊ11.34g/L��22.4L/mol=254g/mol������32x=254
��ã�x=8������ΪS8��
�ʴ�Ϊ��S8��
��2����ͬ״���£���ͬ��������壬��������ʵ�����ͬ������֮�ȵ���Ħ������֮�ȣ�����SX������Ħ������Ϊ6.62��29g/mol=192g/mol������32x=192�����x=6������ΪS6��
�ʴ�Ϊ��S6��
��3����ͬ�����£��ܶ�֮�ȵ��ڵ���Ħ������֮�ȣ�����SX������Ħ������Ϊ2g/mol��64=128g/mol������
32x=128�����x=4������ΪS4��
�ʴ�Ϊ��S4��
���������
�����Ѷȣ�һ��
3��ѡ���� ͬ��ͬѹ�£�ij��������O2��116g��������CO2��122g���ֳ���ij������114g����ij�������Է�������Ϊ
[? ]
A��16
B��60
C��28
D��4
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ͬ��ͬѹ�£���������������ͬ������Ҫԭ����
[? ]
A������ķ��Ӵ�С��ͬ
B��������Ӽ��ƽ�����벻ͬ
C����������ʵ�����ͬ
D����������ʲ�ͬ
�ο��𰸣�C
���������
�����Ѷȣ���
5�������� ��1��a g O2�к�N����ԭ�ӣ����ӵ�����Ϊ________________��
��2���ڱ�״���£�V L H2�к���N������ӣ����ӵ�����Ϊ__________��
��3��m g H2��O2�Ļ�������к���N1������Ӻ�N2�������ӣ����ӵ�����Ϊ________��
��4��������20��ˮΪ1mL��ˮ���ܶ�Ϊ1g/mL��ÿ��ˮ��a��ˮ���ӣ����ӵ�����Ϊ______��
�ο��𰸣���1��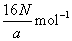 �� ��2��
�� ��2��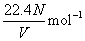 �� ��3��
�� ��3��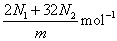 �� ��4��360a mol�D1
�� ��4��360a mol�D1
���������[˼·����] ���⿼�������ʵ���Ϊ���ĵļ��㡣�� ��չ�����㡣
��չ�����㡣
��1���� ��
��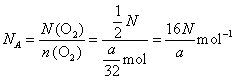 ��
��
��2����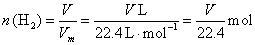 ��
��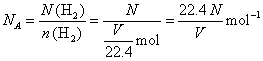 ��
��
��3����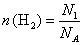 ��
��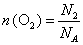 ����n (H2)��M (H2)+n (O2)��M (O2)=m g��֪��
����n (H2)��M (H2)+n (O2)��M (O2)=m g��֪��
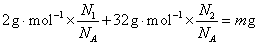 ������֪
������֪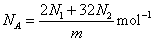 ��
��
��4����1 ��ˮ��������
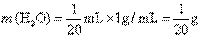 ��
��
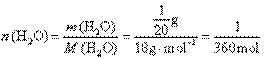 ������
������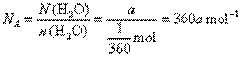 ��
��
��ʾ��Ҫ��ʵ���������ʵ���Ϊ���ġ�
�����Ѷȣ���