1��ѡ���� ���н����ڿ��������Է��γ������ﱣ��Ĥ����
[? ]
A��Fe
B��Al
C��Mg
D��Na
�ο��𰸣�BC
���������
�����Ѷȣ���
2������� ������һ��ǿ������������������������ȣ�
��1��O3��KI��Һ��Ӧ���ɵ����ֵ�����______��______���������ʽ��
��2��O3��ˮ���ֽ⣬һ�������£�O3��Ũ�ȼ���һ�������ʱ�䣨t�����±���ʾ����֪��O3����ʼŨ��Ϊ0.0216mol/L��
pH
t/min
T/�� | 3.0 | 4.0 | 5.0 | 6.0
20
301
231
169
58
30
158
108
48
15
50
31
26
15
7
|
��pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���______��
����30�桢pH=4.0�����£�O3�ķֽ�����Ϊ______mol/��L?min����
�۾ݱ��еĵݱ���ɣ��Ʋ�O3�����������·ֽ��������������˳��Ϊ______��������ĸ���ţ�
a��?40�桢pH=3.0? b��?10�桢pH=4.0? c��?30�桢pH=7.0
��3��O3���ɳ�����������ԭ����ͼ�����ϡ�����Ƶã�
��ͼ������Ϊ______���A����B��������缫��ӦʽΪ______��
����C��ͨ��O2����A���ĵ缫��ӦʽΪ______��
����C����ͨ��O2��D��E���ֱ��ռ���x?L��y?L���壨��״��������E���ռ���������O3��ռ���������Ϊ______������O3�ķֽ⣩��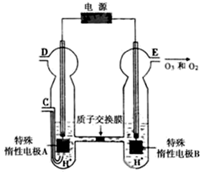
�ο��𰸣���1��O3��KI��Һ��Ӧ���ɵ����ֵ���ֻ��ΪO2��I2���ʴ�Ϊ��O2��I2��
��2����pH������OH-Ũ������pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���OH-���ʴ�Ϊ��OH-��?
��v=��ct=0.0108mol/L108min=1.00��10-4mol/��L?min�����ʴ�Ϊ��1.00��10-4��?
���ɱ������ݿ�֪��40��C��pH=3.0ʱ������ʱ����31min��158min֮�䣻
10��C��pH=4.0 ʱ������ʱ�䣾231nin��
30��C��pH=7.0ʱ������ʱ�䣼7min����ֽ��������������˳��Ϊb��a��c��
�ʴ�Ϊ��b��a��c��
��3��������ͼ��֪��B������O2��O3��B����Ӧ������Ӧ��������������������Ӧ����AΪ�������缫��ӦΪ2H++2e-�TH2����
�ʴ�Ϊ��A��2H++2e-�TH2����
��C��ͨ��O2��O2������ԭ��Ӧ������������������ˮ���缫��ӦʽΪO2+4H++4e-=2H2O���ʴ�Ϊ��O2+4H++4e-=2H2O��
����C����ͨ��O2��ʵ��Ϊ���ˮ��D��Ϊ���������Ϊx?L��E��Ϊ�����������������Ϊy?L������������ΪZL�����ݵ���ת���غ���
x��2=Z��3��2+��y-Z����2��2�����Z=x-2y������E���ռ���������O3��ռ���������Ϊx-2yy��
�ʴ�Ϊ��x-2yy��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ʵ���������ʼ�ֱ��ת����Ԫ����

[? ]
A����
B����
C����
D����
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� ���������ƣ�Ҳ���γɺ�O22-���ӵĹ����������������������ǣ�������
A�����������Ļ�ѧʽ��Ba2O2
B��1mol�������ƻ��������������ˮ��Ӧ������0.5mol����
C���������������ӻ�����
D���������ƻ������������ǿ������
�ο��𰸣�A����Ϊ��Ԫ����+2�ۣ���Ba 2+��O22-������-2�ۣ����Թ���������ֻ����BaO2����A����
B����������ƻ����������ˮ��Ӧ��2H2O+2Na2O2=4NaOH+O2����2H2O+2BaO2=2Ba��OH��2+O2��������1mol�������������ˮ��Ӧ������0.5mol��������B��ȷ��
C��������������ɻ��õĽ�����ǽ���Ԫ����ɵ����ӻ������C��ȷ��?
D��������������е���Ϊ-1�ۣ�����ǿ�����ԣ���D��ȷ��
��ѡA��
���������
�����Ѷȣ���
5��ѡ���� ���������ƽ�������ʵ�飬������������������
[? ]
A������Ͷ�뵽����ˮ��
B���������������ò���һЩС�ף��ٷ���������ˮ��
C�����Ʒ�������ϡ������
D�����Ʒ�������ϡ������
�ο��𰸣�B
���������
�����Ѷȣ�һ��