1、选择题 下列离子反应方程式中,属于水解反应的是
A.CN-+H2O HCN+OH-
HCN+OH-
B.NH3・H2O NH4++OH-
NH4++OH-
C.HCO3-+H2O H3O++CO32-
H3O++CO32-
D.H2CO3 HCO3-+H+
HCO3-+H+
参考答案:A
本题解析:
正确答案:A
B、电离;C、电离;D、电离。
本题难度:一般
2、选择题 已知H2PO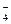 以电离为主。在0.1mol・L-1的NaH2PO4溶液中,下列粒子浓度关系不正确的是()
以电离为主。在0.1mol・L-1的NaH2PO4溶液中,下列粒子浓度关系不正确的是()
A.c(Na+)+c(H+)=c(OH-)+c(H2PO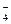 )+2c(HPO
)+2c(HPO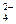 )+3c(PO
)+3c(PO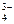 )
)
B.c(H3PO4)+c(H+)=c(OH-)+c(HPO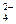 )+2c(PO
)+2c(PO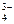 )
)
C.c(Na+)=c(H2PO-4)+3c(PO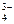 )+2c(HPO
)+2c(HPO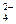 )+c(H3PO4)?
)+c(H3PO4)?
D.c(Na+)>c(H2PO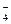 )>c(H+)>c(HPO
)>c(H+)>c(HPO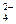 )>c(H3PO4)
)>c(H3PO4)
参考答案:C
本题解析:A是电荷守恒,B是物料守恒D.NaH2PO4溶液中离子浓度的大小判断正确(可结合前面的要点2)。
本题难度:简单
3、选择题 下列方程式中,属于水解反应的是(?)
A.H2O + H2O  H3O+ + OH―
H3O+ + OH―
B.HCO3― + OH― ="" H2O + CO32―
C.CO2 + H2O  H2CO3
H2CO3
D.CO32― + H2O  HCO3― + OH―
HCO3― + OH―
参考答案:D?
本题解析:属于水解反应的只有D选项
本题难度:简单
4、选择题 在盐类的水解过程中,下列各种情况必定发生的是
A.盐的电离平衡被破坏
B.水的电离平衡被破坏
C.25℃,溶液的pH不是7
D.溶液温度升高
参考答案:B
本题解析:盐的水解本质上是弱酸或弱碱的离子与水电离的氢离子或氢氧根离子结合,打破水的电离平衡,故答案为B。
本题难度:简单
5、选择题 分别将下列物质:①CuSO4 ②Na2O2 ③NaCl ④Ca(HCO3)2 ⑤FeCl3投入水中,对其溶液加热蒸干,仍能得到原物质的是(?)
A.①②③
B.①③
C.③④
D.③
参考答案:B
本题解析:①CuSO4是难挥发的强酸弱碱盐,溶液蒸干得到的任然是该物质本身。正确。②Na2O2放入水中发生反应得到的是NaOH。把溶液蒸干得到的是NaOH。错误。③NaCl是强酸强碱盐,在溶液中不水解。溶液蒸干得到的NaCl.正确。④Ca(HCO3)2是强碱弱酸盐,加热时水解产生的弱酸H2CO3会与碱发生反应Ca(OH)2得到正盐CaCO3。CaCO3难溶于水,所以把溶液蒸干得到的是CaCO3。错误。⑤FeCl3该盐水解FeCl3+3H2O  Fe(OH)3+3HCl产生的HCl有挥发性,会随着水分的蒸发而挥发,促使盐继续水解,最终得到的是Fe(OH)3。错误。
Fe(OH)3+3HCl产生的HCl有挥发性,会随着水分的蒸发而挥发,促使盐继续水解,最终得到的是Fe(OH)3。错误。
本题难度:一般