1、选择题 a.b.c.d.e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
A.baedc
B.edabc
C.abdce
D.cdeab
参考答案:a和b的最高价氧化物对应水化物呈碱性,则a、b为金属,且失电子能力b>a(其最高价氧化物对应水化物的碱性b>a);
c和d的气态氢化物的还原性d>c,即c、d为非金属,且得电子能力d<c.
根据同周期元素从左到右失电子能力逐渐减弱,得电子能力逐渐增强的规律,将a、b、c、d四种元素大致排序为: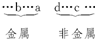 因为五种元素的原子得失电子后所形成的简单离子中e的离子半径最小,则e应为金属元素,且原子序数b<a<e(如Na、Mg、Al).
因为五种元素的原子得失电子后所形成的简单离子中e的离子半径最小,则e应为金属元素,且原子序数b<a<e(如Na、Mg、Al).
故选A.
本题解析:
本题难度:一般
2、选择题 由短周期元素构成的某离子化合物X中,一个阳离子和一个阴离子核外电子数之和为20.则有关X的下列说法中正确的是( )
A.X中阳离子和阴离子个数不一定相等
B.X中一定有离子键,一定不含共价键
C.若X只含两种元素,则这两种元素可在同一周期也可在同一主族
D.X中阳离子半径一定大于阴离子半径
参考答案:由题意知阴、阳离子均是10电子微粒,它们可以是:阴离子:N3-、O2-、F-、OH-等,阳离子:NH4+、Na+、Mg2+、Al3+等.
A、当阴、阳离子所电荷不相等,阳离子和阴离子个数不相等,如、MgF2、Na2O,当阴、阳离子所电荷相等,阳离子和阴离子个数相等,如NaF、NaOH,故A正确;
B、X是离子化合物,一定有离子键,也可能含共价键,如NaOH、Mg(OH)2、NH4F等,故B错误;
C、若X只含两种元素可以是NaF、MgF2、Na2O、Na3N等,两元素不能在同一周期也不能在同一主族,故C错误;
D、对简单的离子,阴、阳离子电子层结构相同,核电荷数越大,离子半径越小,阳离子的核电荷数一定大于阴离子的核电荷数,所以X中阳离子半径小于阴离子半径,故D错误.
答案:A
本题解析:
本题难度:简单
3、选择题 两种元素的原子的核外电子层数之比与最外层电子之比相等,则在1-10号元素中满足上述条件的元素共有
[? ]
A.1对
B.2对
C.3对
D.4对
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列说法中正确的是( )
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
参考答案:A.非金属元素呈现的最高化合价等于原子最外层电子数,不超过该元素原子的最外层电子数,故A正确;
B.非金属元素呈现的最低化合价为原子最外层电子数-8,最高化合价等于原子最外层电子数,故B错误;
C.He最外层电子数为2,为非金属元素,故C错误;
D.最外层有5个电子的原子位于周期表第ⅤA族,第ⅤA元素既有金属元素也有非金属元素,故D错误.
故选A.
本题解析:
本题难度:一般
5、简答题 不同元素的原子在分子内吸引电子的能力大小可用x表示,x越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的x值.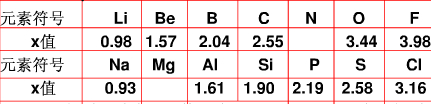
(1)通过分析x值的变化规律,确定Mg、N的x值范围
Mg:______、N:______.
(2)短周期元素x值的变化特点体现了元素性质的______变化规律.
(3)某有机物分子中含有S-N键,你认为电子对偏向______原子(填元素符号).
(4)经验规律告诉我们,当成键的两原子相应元素的x差值△x大于l.7时一般形成离子键,△x小于1.7时一般形成共价键,试预测:AlBr3中化学键的类型是______.设计实验验证你的预测______.
参考答案:(1)根据电负性的递变规律:同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,可知,在同周期中电负性Na<Mg<Al,同主族Be>Mg>Ca,最小范围应为0.93~1.57;同理,在同周期中电负性C<N<O,同主族N>P,
最小范围应为2.55~3.44;故答案为:0.93~1.57;2.55~3.44.
(2)因每隔一定数目的原子,元素的电负性逐渐增大,这种变化称为周期性,故答案为:周期性.
(3)因N的电负性大于S的电负性,所以N吸引电子的能力强,故答案为:N.
(4)因同主族,电负性逐渐减小,故Br的电负性小于3.16,所以AlBr3中Al与Br的电负性差值<1.55,根据信息,电负性差值若小于1.7,则形成共价键,所以AlBr3为共价化合物.离子化合物在熔融状态下以离子形式存在,可以导电,但共价化合物不能导电.故答案为:共价键;测定熔融状态下是否导电,若不导电则为共价键.
本题解析:
本题难度:一般