1、填空题 (6分)某双原子分子构成的气体,其摩尔质量为M (g・mol-1),已知阿伏加德罗常数为NA (mol-1),标准状况下气体摩尔体积为Vm (L・mol-1),现有质量为n g的该气体,则:
(1) 该气体的物质的量为 mol。
(2) 该气体在标准状况下的体积为 L。
(3) 该气体所含原子总数为 个。
参考答案:n/M, nVm/M, 2nNA/M (每空2分)
本题解析:考查物质的量的有关计算。
(1)根据n=m/M可知,该气体的物质的量为n/Mmol。
(2)根据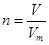 可知,标准状况下的体积是n/Mmol×Vm L・mol-1=nVm/ML
可知,标准状况下的体积是n/Mmol×Vm L・mol-1=nVm/ML
(3)用于分子是双原子分子,所以该气体所含原子总数为n/M×2×NA=2nNA/M。
本题难度:一般
2、选择题 用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A.标准状况下,22.4?L?CO2含有的分子数为?NA
B.将10.6?g?Na2CO3溶于水,电离出Na+的数目为0.2?NA
C.1?mol?CuO被还原成Cu,得到电子数目为2?NA
D.1?L?0.5?mol/L的FeCl3溶液中,含有Cl-?数目为?0.5?NA
参考答案:A、标准状况下,22.4 L CO2物质的量为1mol,含有的分子数为NA,故A正确;
B、10.6 g Na2CO3物质的量为0.1mol,溶于水电离出钠离子数为0.2NA,故B正确;
C、1 mol CuO被还原成Cu,铜元素化合价从+2价变化为0价,得到电子数目为2NA,故C正确;
D、1 L 0.5 mol/L的FeCl3溶液中,含有Cl- 数目为1.5NA,故D错误;
故选D.
本题解析:
本题难度:简单
3、选择题 下列各物质中,含氧原子个数最多的是( )
A.1molKClO3
B.0.5molH3PO4
C.32g?O2
D.3.01×1023个CO2
参考答案:A、1molKClO3中含氧原子物质的量为3mol;
B、0.5molH3PO4中含氧原子物质的量为2mol;
C、32gO2物质的量为1mol,含氧原子物质的量为2mol;
D、3.01×1023个CO2 物质的量0.5mol,含氧原子物质的量为1mol;
综上所述A中含氧原子数最多;
故选A.
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.在标准状况下22.4L?H2中含有氢分子的个数为2NA
B.24g?Mg变为Mg2+时失去的电子数为2NA
C.32g?O2中含有氧原子的个数为2NA
D.1L?1mol/L?NaCl溶液中含有钠离子的个数为NA
参考答案:A、在标准状况下22.4L?H2物质的量为1mol,含有氢分子的个数为NA,故A错误;
B、24g?Mg物质的量为1mol,原子最外层电子为2,变为Mg2+时失去的电子数为2NA,故B正确;
C、32g?O2物质的量为1mol,分子中含有氧原子的个数为2NA,故C正确;
D、1L?1mol/L?NaCl溶液中含有氯化钠1mol,氯化钠全部电离成氯离子和钠离子,钠离子的个数为NA,故D正确;
故选A.
本题解析:
本题难度:一般
5、选择题 NA代表阿伏加德罗常数,下列叙述错误的是( )
A.2mol乙醇和1mol乙二酸反应生成乙二酸二乙酯时,生成的水分子数为2NA
B.3.2g?N2H4中共用电子对的数目为0.5NA
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.同温下,1L?0.5mol?L-1NH4Cl溶液与2L?0.25mol?L-1NH4Cl溶液含NH4+物质的量不同
参考答案:A、2mol乙醇和1mol乙二酸反应生成乙二酸二乙酯时,反应是可逆反应,不能进行彻底,生成的水分子数小于2NA,故A错误;
B、3.2g N2H4中物质的量为0.1mol,每个氮原子形成三个共价键,分子中共用电子对的数目为0.5NA,故B正确;
C、标准状况下,分子数为NA的CO、C2H4混合气体物质的量为1mol,体积约为22.4L,摩尔质量相同为28g/mol,所以质量为28g,故C正确;
D、铵根离子水解,难度不同水解程度不同,则同温下,1L 0.5mol?L-1NH4Cl溶液与2L 0.25mol?L-1NH4Cl溶液含NH4+物质的量不同,故D正确;
故选A.
本题解析:
本题难度:一般