|
�߿���ѧ�ؿ�֪ʶ�㡶ˮ�ĵ���ƽ�⡷����̣�2019�����°棩(ʮ)
2019-07-03 23:33:12
�� �� �� ��
|
1��ѡ���� 50��ʱ�����и���Һ�У����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����
A��pH=4�Ĵ����У�c��H+��=4��0molL��1
B������С�մ���Һ�У�c��Na+��= c��HCO3����
C������ʳ��ˮ�У�c��Na+��+ c��H+��= c��Cl����+c��OH����
D��pH=12�Ĵ�����Һ�У�c��OH����=1��0��10��2mol?L��1
|
�ο��𰸣�C
���������A��pH=4�Ĵ����У�c��H+��=10��4mol��L��1������B�����������غ�֪������С�մ���Һ�У�c��Na+��= c��HCO3����+ c��CO32����+ c��H2CO3��������C�����ݵ���غ�֪������ʳ��ˮ�У�c��Na+��+ c��H+��= c��Cl����+c��OH��������ȷ��D��50��ʱKw��1��10��14��pH=12�Ĵ�����Һ�У�c��OH������1��0��10��2mol?L��1������
���㣺����pH���㡢��Һ������Ũ�ȴ�С��ϵ��
�����Ѷȣ�һ��
2������� ��1����pH= a��CH3COOH��Һϡ��100����������ҺpH a +2�������������
��0.01mol/LCH3COOH��Һ��pH 2���������������
��0.1mol/LCH3COONa��Һ��pH 7���������������
��2��ij��������Na2CO3��NaOH��MgCl2��AlCl3��BaCl2��Fe2(SO4)3��(NH4)2SO4�е����ֻ�϶��ɡ�ȡ�ù�������ˮ�õ���ɫ������Һ�������Һ�м���ϡ���ᣬ�а�ɫ�������ɣ���������ϡ���ᣬ��������ȫ��ʧ��������������������������� ԭ�����к��������� �� ����д��ѧʽ��
�ο��𰸣���1���� �� �� �� �� �� ��
��2��NaOH �� AlCl3
�����������1������ΪCH3COOHΪ���ᣬϡ��ʱ����ƽ�������ƶ�������pH= a��CH3COOH��Һϡ��100����������ҺpH��a +2��
�ڴ����ȫ���룬����0.01mol/LCH3COOH��Һ��pH��2��
��CH3COONaΪ����ǿ���Σ�ˮ���Լ��ԣ�����0.1mol/LCH3COONa��Һ��pH��7��
��2������ˮ�õ���ɫ������Һ��˵������Fe2(SO4)3�������Һ�м���ϡ���ᣬ�а�ɫ�������ɣ���������ϡ���ᣬ��������ȫ��ʧ�������������������������˵��ԭ�����к���NaOH��AlCl3��
���㣺���⿼����Һ����Ե��жϡ����ʵ��ƶϡ�
�����Ѷȣ�����
3��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A��ʯ������Na2CO3��Һ��ϣ�Ca2++CO32-=CaCO3
B��NH4HSO3��Һ��������NaOH��Һ��ϼ��ȣ�NH4++HSO3-+2OH- NH3��?+SO32-+2H2O
C������������KIO3��Һ��KI��Һ������Ӧ����I2��IO3-+5I-+3H2O=3I2+6OH-
D��AgNO3��Һ�м�������İ�ˮ��Ag++NH3?H2O=AgOH+NH4+
�ο��𰸣�
A��ʯ������Na2CO3��Һ��ϣ���ȷ�����ӷ���ʽΪ��Ca��OH��2+CO32-=CaCO3��+2OH-����A����
B��NH4HSO3��Һ��������NaOH��Һ��ϼ��ȣ�������NaOH��Һ�������OH-������NH4+��Ӧ������HSO3-��Ӧ������ʽ���Ͽ���ʵ����ѧʽ��д��ȷ����ɺ�ԭ�Ӷ��غ㣮��B��ȷ��
C������������KIO3��Һ��KI��Һ������Ӧ����I2����ȷ�����ӷ���ʽΪ��IO3-+5I-+6H+=3I2+3H2O����C����
D��AgNO3��Һ�м��������İ�ˮ��������Ӧ��Ag++NH3?H2O�TAgOH��+NH4+ ?�ӹ����İ�ˮ��������Ӧ��AgOH+2NH3?H2O�T[Ag��NH3��2]++2H2O+OH-����D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ��pH=2��CH3COOH��Һ����pH=2��H2SO4��Һ����pH=12�İ�ˮ����pH=12��NaOH��Һ����ͬ�����£��й�������Һ�ıȽ��У���ȷ���ǣ�������
A�����ڡ�����Һ��Ϻ�pH=7��������Һ��������ڣ���
B����10mL����������Һ�и�����90mL��ˮ����Һ��pH���ۣ��ܣ��٣���
C��ˮ�����c��H+������=��=��=��
D��������Ģ١��ڡ�����Һ�ֱ����������۷�Ӧ������H2�����������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� ��6�֣���֪ij�¶���CH3COOH�ĵ��볣��K=1.6��10-5�����¶�����20mL0.01mol/LCH3COOH��Һ����μ���0.01mol/L KOH��Һ����pH�仯��������ͼ��ʾ�������¶ȱ仯������ش������й����⣺
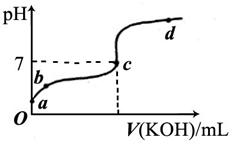
��1��a����Һ��c(H+)Ϊ ��
��2��b����Һ������Ũ�ȵĴ�С˳������� �������
��3��a��b��c������ˮ�ĵ���̶������� ��
�ο��𰸣���1��4��l0-4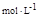 ��2��3 ��3��c ��2��3 ��3��c
�����������1��K=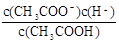 ����Һ�е�c(CH3COO-)=c(H+)������c(H+)= ����Һ�е�c(CH3COO-)=c(H+)������c(H+)=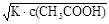 =4��l0-4 =4��l0-4 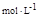 �� ��
��2��b����Һ�����ԣ��������c(CH3COO-)>c(H+)>c(K+)>c(OH-)��c(CH3COO-)>c(K+))>c(H+)>c(OH-)��c(CH3COO-)>c(H+)=c(K+)>c(OH-)���������
��3����������ˮ�ĵ��룬�������δٽ�ˮ�ĵ��룬����c��ˮ�ĵ���̶����
���㣺������ʵĵ���
�����������ѶȽϴ��ɵ���ƽ�ⳣ����c(H+)ʱ��Ҫע������ѵ�����ᡣ
�����Ѷȣ�һ��
|