1、简答题 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜反应的情况,回答下列问题:
(1)我们知道,稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解.该反应的化学方程式为______.某同学未加入氧化剂,而是将它设计成一个电解装置,也能使铜很快溶于稀盐酸.请在方格中画出该装置:
(2)在一定体积的18mol?L-1的浓硫酸中加入过量的铜片,加热使之反应,被还原的硫酸是0.9mol,则该硫酸的实际体积______(填大于、等于或小于)100mL.有同学提出:若使剩余的铜片继续溶解,可向其中加入硝酸盐,可行吗?______(填“可行”或“不可行”).如果可行,用离子方程式说明原因;如果不可行,此问可以不填______.
(3)将等质量的铜片分别与等体积、过量的浓硝酸和过量的稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?______(填“同意”或“不同意”),原因是______.另一同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否,请简述实验方案、实验现象及由此得出的结论:______.
参考答案:
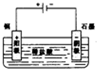
(1)双氧水具有氧化性,在酸性环境下能将金属铜氧化,方程式为:Cu+H2O2+2HCl=CuCl2+2H2O,用电解原理实现铜和盐酸的反应,根据电解原理阳极必须是金属铜,电解质必须是稀盐酸,故答案为:Cu+H2O2+2HCl=CuCl2+2H2O;
(2)铜只能和浓硫酸反应和稀硫酸不反应,Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+H2O,随着铜和浓硫酸的反应的进行,酸的浓度越来越小,不再产生二氧化硫,当被还原的硫酸是0.9mol,则18mol?L-1的浓硫酸的实际体积要大于100mL;若使剩余的铜片继续溶解,可向其中加入硝酸盐,应为溶液中有H+,再加入硝酸盐引入NO3-,相当于存在了硝酸,硝酸能将同溶解,反应实质为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:大于;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)将等质量的铜片分别与等体积、过量的浓硝酸和过量的稀硝酸反应后,所得溶液中Cu2+的浓度基本相等,颜色基本相同,若溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,可以向蓝色溶液中通入一定量的NO2来检验,
故答案为:不同意;等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等;将一定量的NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确.
本题解析:
本题难度:一般
2、选择题 已知酸性条件下有反应:2Cu+ = Cu2++Cu。氢气还原氧化铜实验由于反应温度不同,产物可能不同。下表为在红色的还原产物中加入试剂和产生的现象。
由此推出本次氢气还原氧化铜实验的产物是

[? ]
A.是Cu
B.是Cu2O
C.一定有Cu,可能有Cu2O
D.一定有Cu2O,可能有Cu
参考答案:D
本题解析:
本题难度:一般
3、选择题 下表各组物质中,满足下图物质一步转化关系的选项是( )

A.Na? NaOH? NaHCO3
B.Cu? CuSO4? Cu(OH)2
C.C CO CO2
D.Si? SiO2? H2SiO3
参考答案:C
本题解析:
本题难度:简单
4、选择题 向铁和铜的混合物中加入一定量的稀硫酸,反应后剩余了m1克金属,再继续加入一定量的硝酸钠溶液后剩余了m2克金属,则m1和?m2的大小关系正确的是( )
A.m1=m2
B.m1>m2
C.m1<m2
D.m1≥m2
参考答案:D
本题解析:
本题难度:简单
5、选择题 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响)。则滴管和烧瓶中所用试剂可能是
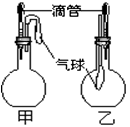
[? ]
甲
乙
A.
稀硫酸和铜片
浓氨水和SO2
B.
双氧水和MnO2
NaOH溶液和CO2
C.
NaHCO3溶液和苯酚
NaOH溶液和Cl2
D.
H2O和NH3?
NaOH和SO2
参考答案:B
本题解析:
本题难度:简单