1、选择题 某元素为非金属元素,该元素的原子结合一个电子即达到稳定结构,则下列关于该元素的描述中一定正确的是( )
A.第ⅦA族的卤素
B.主族元素
C.副族元素
D.单质有很强的氧化性
参考答案:B
本题解析:
本题难度:简单
2、选择题 A、B是两种同主族元素的原子,当它们都获得2个电子形成稳定结构的阴离子时,A放出的能量大于B,由此可知( )
A.氢化物稳定性:H2A>H2B
B.还原性:A2->B2-
C.原子半径:A>B
D.非金属性:A<B
参考答案:A与B两种元素的原子,当它们分别获得2个电子形成稳定结构的阴离子,说明最外层都有6个电子,位于周期表第ⅥA族,A放出的能量大于B,说明A的非金属性大于B,则原子序数A小于B,则
A.A的非金属性大于B,则A的氢化物的稳定性大于B,故A正确;
B.素的非金属性越强,对应阴离子的还原性越弱,则B-还原性大于A-,故B错误;
C.原子序数A小于B,二者在同一主族,则A的原子半径小于B,故C错误;
D.同主族元素A、B获得2个电子形成稳定结构的阴离子时,A放出的能量大于B,说明A的非金属性大于B,故D错误.
故选A.
本题解析:
本题难度:简单
3、选择题 下列说法中正确的是
[? ]
A.原子核都是由质子和中子构成
B.质子数相同的粒子其化学性质不一定相同
C.某种粒子最外层上有8个电子,则一定是稀有气体元素的原子
D.粒子的价电子构型为ns2np6,则为稀有气体元素
参考答案:B
本题解析:
本题难度:简单
4、填空题 X、Y、Z是中学化学常见的三种元素,其中,X、Z位于短周期.常温下,X单质为黄绿色气体;向含Y离子的溶液中滴加氢氧化钠溶液,生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色;Z的最外层电子数与核外电子总数之比为3:13.请回答下列问题:
(1)Z在元素周期表中的位置是______,X单质分子的电子式是______.
(2)Z单质与Y的氧化物在高温条件下反应是冶炼Y单质的一种方法,该反应化学方程式是______.
(3)含上述元素的某些物质常用于处理工业废水,部分流程如图1:
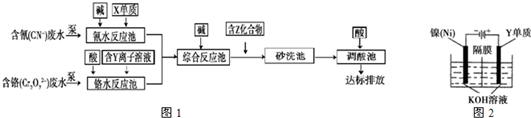
①处理含铬废水时,在反应池中Cr2O72-变为Cr3+,当反应转移1mol?电子时,有______?mol?Cr2O72-?转化(计算结果保留两位小数).
②含Z化合物可以使水中悬浮颗粒发生凝聚,原因是______(用文字和化学用语表示).
③处理含氰废水时,CN-最终转化为两种无毒的气体,该反应的离子方程式是______.
(4)利用图2方法电解可得到一种新型净水剂K2YO4,阳极的电极反应式为______.
参考答案:常温下,X单质为黄绿色气体应为Cl2,则X为Cl元素,向含Y离子的溶液中滴加氢氧化钠溶液,生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色,该红色沉淀为Fe(OH)3,则Y为Fe元素,Z的最外层电子数与核外电子总数之比为3:13,应为Al元素,
(1)Z为Al元素,原子核外有3个电子层,最外层电子数为3,则应位于周期表三周期ⅢA族,X单质为Cl2,电子式为

,
故答案为:三周期ⅢA族,

;
(2)Z单质与Y的氧化物在高温条件下反应是冶炼Y单质,为Al和铁的氧化物的反应,为铝热反应,反应的可能方程式为Fe2O3+2Al?高温?.?Al2O3+3Fe或3Fe3O4+8Al?高温?.?4Al2O3+9Fe或3FeO+2Al?高温?.?Al2O3+3Fe,
故答案为:Fe2O3+2Al?高温?.?Al2O3+3Fe或3Fe3O4+8Al?高温?.?4Al2O3+9Fe或3FeO+2Al?高温?.?Al2O3+3Fe;
(3)①Cr2O72-变为Cr3+,化合价由+6价降低到+3价,当有1mol电子转移时,应有13molCr被还原,则有16molCr2O72-被还原,即0.17mol,
故答案为:0.17;
②铝离子易水解产生氢氧化铝,反应的离子方程式为Al3++3H2O

Al(OH)3+3H+,氢氧化铝胶体,能吸附水中悬浮物,使之沉淀下来,
故答案为:Al3++3H2O

Al(OH)3+3H+,铝离子水解产生氢氧化铝胶体,能吸附水中悬浮物,使之沉淀下来;
③两种无毒的气体为二氧化碳和氢气,而反应物为CN-和Cl2,则反应氧化还原反应,反应的离子方程式为2CN-+5Cl2+8OH-=2CO2+N2+H2O+10Cl-,
故答案为:2CN-+5Cl2+8OH-=2CO2+N2+H2O+10Cl-;
(4)阳极发生氧化反应,Fe被氧化为FeO42-,电极反应式为Fe-6e-+8OH-=FeO42-+4H2O,
故答案为:Fe-6e-+8OH-=FeO42-+4H2O.
本题解析:
本题难度:一般
5、选择题 X、Y、Z、W都是短周期元素,核电荷数依次增大.X和Z同主族,Y、Z、W同周期,Y的原子半径是所处周期中最大的,W的最高价氧化物所对应的水化物是强酸,X与W的核电荷数之比为3:8.据此判断下列说法正确的是( )
A.Y是第三周期ⅦA族元素
B.非金属性:W>X
C.Z一定是金属元素
D.Y与W的最高正价之和为8
参考答案:X、Y、Z、W都是短周期元素,核电荷数依次增大,Y的原子半径是所处周期中最大,则Y处于ⅠA族,X和Z同主族,故X处于第二周期,Z处于第三周期,Y、Z、W同周期,故Y为Na元素;W处于第三周期,W的最高价氧化物所对应的水化物是强酸,X与W的核电荷数之比为3:8,故W为S元素,X为C元素;X和Z同主族,故Z为Si元素.
A、Y为Na元素,处于第三周期第ⅠA族,故A错误;
B、X为C元素,W为S元素,非金属性S>C,故B正确;
C、Z为Si元素,属于非金属元素,故C错误;
D、Y为Na元素,W为S元素,二者的最高正价之和为7,故D错误;
故选B.
本题解析:
本题难度:一般