1、填空题 写出铝单质与强酸、强碱溶液反应的离子方程式,并标出电子转移的方向和数目:________、____ ____。日常生活中接触到的易拉罐有铁质和铝质之分,听装啤酒是铝质易拉罐,向一只充满二氧化碳气体的铝质易拉罐中加入适量的氢氧化钠溶液,并及时堵住,观察到的现象是____ ,用化学方程式表示产生这一现象的原因是___ 。若用薄铁质易拉罐做上述实验出现的结果是____。
参考答案: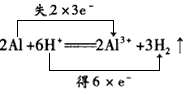 ;
;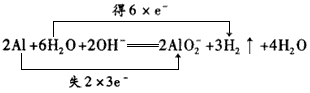 ;
;
易拉罐先瘪下去,一会儿又鼓起来 ;CO2+2NaOH=Na2CO3+H2O, 2Al+2H2O+2NaOH=2NaAlO2+3H2↑ ;薄铁质易拉罐瘪下去后,不再重新鼓起
本题解析:
本题难度:一般
2、选择题 下列各组物质与其用途的关系不正确的是
[? ]
A.过氧化钠:供氧剂
B.烧碱:治疗胃酸过多的一种药剂
C.氧化铝:耐火坩埚
D.明矾:净水剂
参考答案:B
本题解析:
本题难度:简单
3、选择题 向含有amolAlcl3的溶液中加入含b mol KOH的溶液中,生成沉淀的物质的量可能是
[?]
①a mol ② b mol ③ a/3 mol ④b/3 mol ⑤0 mol ⑥ (4a-b) mol
A. ①②③④⑤⑥
B. ①③④⑤⑥
C. ①②③⑤⑥
D. ①③⑤
参考答案:B
本题解析:
本题难度:一般
4、填空题 (16分)某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应
后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色。
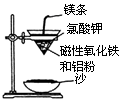
①出现这种现象的原因,除了因“铁块”中可能混有没反应完的
磁性氧化铁外,还有一种可能原因是 ?。
② 若要证明反应所得“铁块”中含有金属铝,可用?(填化学式)溶液,所发生反应的离子方程式为 ?。
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H+ + 4I-+ O2 = 2I2 + 2H2O。该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率。已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深。
实验小组拟用0.8 mol・L-1 KI溶液、0.1 mol・L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A―C三组实验,部分实验数据如下表:
编号
| 温度/℃
| H2SO4体积/mL
| KI溶液体积/mL
| H2O体积/mL
| 淀粉溶液
/ mL
| 出现蓝色时间 /s
|
A
| 39
| 10
| 5
| 5
| 1
| 5
|
B
| TB
| 10
| 5
| 5
| 1
| 没出现蓝色
|
C
| 5
| 10
| 5
| 5
| 1
| 39
|
D
| ?
| ?
| ?
| ?
| ?
| t
|
①为确保A组实验在39℃下进行,应采用的控温操作方法是?。
②A―C三组实验时,都加入了5mL水,其目的是?。
③B组实验中“没出现蓝色”,原因是?。
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标。
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结
论?。
参考答案:(16分,每空2分)
(1)①生成的铁又有一部分被空气氧化
②NaOH(回答其它强碱也得分),2Al+2OH-+2H2O=2AlO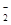 +3H2↑。
+3H2↑。
(2)①将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度
②为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变(凡表达出“控制变量”、“对比实验”意思的各种合理答案都得分)
③温度(TB)高于75℃,淀粉与碘不显色。
D
39或5
10加减5范围内的一个数值
5
5减加5范围内的一个数值
1
?
④
(温度必须为39℃或5℃,KI溶液体积必须为5ml,淀粉溶液为1ml,水和硫酸溶液总体积为20ml的各种组合答案均得分)。
⑤设计酸体积<10mL时,t预测值要大于同温对比值;设计酸体积>10mL时,t预测值要小于同温对比值(合理范围内的数值都给1分)。结论为:酸度越大反应速率越快(1分)(若得出结论为:酸度越大反应速率越慢,不给分)。
本题解析:(1)①使KSCN溶液变红色说明溶液中存在铁离子,除铁块中含有未反应的磁性氧化铁外,另一原因是:因为该反应是在高温下进行的,生成的单质铁又与空气中的氧气发生氧化还原反应生成了氧化铁,与盐酸反应,溶液中有了铁离子而使KSCN溶液变红;
②证明铁块中含有铝,需选择强碱溶液如NaOH溶液,因为铁不与氢氧化钠溶液反应,而铝与氢氧化钠溶液反应产生气体;反应的离子方程式为2Al+2OH-+2H2O=2AlO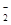 +3H2↑。
+3H2↑。
(2)①控制温度恒温的最好操作是水浴加热,具体操作是:将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度
②本实验的目的是探究温度、酸度对上述反应速率的影响,所以A―C三组实验时,都加入了5mL水,目的是为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变;
③根据已知:淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;所以B组实验中“没出现蓝色”,原因是温度高于75℃,淀粉与碘不显色。
④前三组实验的数据表明是在酸度相同时,探究温度对反应速率的影响,所以D组应是当温度相同时,探究酸度对反应速率的影响,乙组实验现象不正确,应舍弃,所以D组的温度与甲或丙是相同的,为保证淀粉的浓度是相同的,所以硫酸和水的总体积是15mL,再去改变硫酸溶液和水的体积来改变溶液的酸度,判断出现蓝色的时间,具体数据如下:
D
39或5
10加减5范围内的一个数值
5
5减加5范围内的一个数值
1
?
⑤依据酸的体积确定溶液的酸度,由4H+ + 4I-+ O2 = 2I2 + 2H2O可知,溶液酸度越大,生成碘的速率越快,与同温度的实验相比,看到蓝色的时间越短。
本题难度:一般
5、选择题 下列从海水中提取镁正确的方法是(?)
(提示:熔点:MgO 2 850℃ MgCl2 714℃)
A.海水 Mg(OH)2
Mg(OH)2 Mg
Mg
B.海水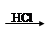 MgCl2溶液→MgCl2晶体
MgCl2溶液→MgCl2晶体 Mg
Mg
C.海水 Mg(OH)2
Mg(OH)2 MgO
MgO Mg
Mg
D.海水 Mg(OH)2
Mg(OH)2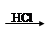 MgCl2溶液→MgCl2晶体
MgCl2溶液→MgCl2晶体 Mg
Mg
参考答案:D
本题解析:首先是富集,海水加石灰乳生成Mg(OH)2沉淀、洗涤,洗涤后加盐酸生成MgCl2,因MgO熔点比MgCl2高,故电解MgO耗能多不经济,应电解MgCl2。
本题难度:简单