1��ѡ���� ��֪�����£�Al(OH)3��KspԶ����Fe(OH)3����Ũ�Ⱦ�Ϊ0.1mol/L��Fe(NO3)3��Al(NO3)3�����Һ�У���μ���NaOH��Һ������ʾ��ͼ��ʾ����Al(OH)3�����ʵ��������NaOH��Һ�������ϵ����������(? )
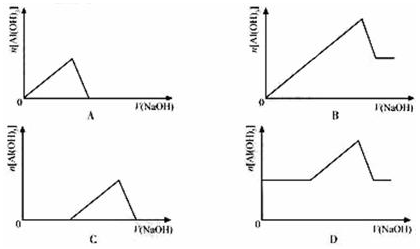
�ο��𰸣�C
��������������£�Al(OH)3��KspԶ����Fe(OH)3��Al(OH)3���ܽ�ȴ����Լ���NaOH������Fe(OH)3������Fe(NO3)3��ȫ�������ٺ�Al(NO3)3��Ӧ����Al(OH)3�������μ�NaOH�����ܽ⡣����ͼ��ѡC��
�����Ѷȣ�һ��
2��ѡ���� 11.9gMg��Al��Fe��ɵĺϽ��ܽ���������NaOH��Һ���Ͻ���������2.7g����ȡ�������ĺϽ��ܽ��������������У���Ӧ�������״���µ�6.72LNO����������Һ�м���������NaOH��Һǡ��ʹ��������ת��Ϊ�����������Ϊ��?��g
A��22.1
B��27.2
C��30
D��14.6
�ο��𰸣�B
������������Ͻ����ڹ���ϡ�����У��ֱ�����Al3+��Fe3+��Mg2+���ӣ����ݵ����غ㣬������ʧȥ���ӵ����ʵ���Ϊ6.72L/��22.4L/mol����3=0.9mol����Ӧ�н���ʧȥ���ӵ����ʵ����������ɼ�����������ӵ����ʵ�������n��OH-��=0.9mol�����Է�Ӧ���������������11.9g+0.9mol��17g/mol=27.2g����ѡB��
����������������û�ѧ����ʽһ��һ������û��������кܴ�ļ����������Կ����������ĵ���غ������㣬���ǽ��⼼��֮һ��
�����Ѷȣ���
3������� ij��ѧ��ȤС��ģ�ҵ�ϴ���������Ҫ�ɷ���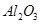 ����
����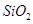 ��
��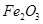 �����ʣ�����ȡ�������Ĺ�����ʵ�飬�������£�
�����ʣ�����ȡ�������Ĺ�����ʵ�飬�������£�
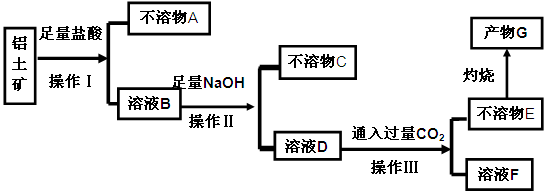
��ش��������⣺
��1�������������Ϊ?��
��2����֤��ҺB���Ƿ���Fe3+�ķ�����?��
��3��������A��?(�ѧʽ)��д��D��E��Ӧ�����ӷ���ʽ?��
��4��˵����ҺF�к�̼Ԫ�����ʵ�һ����;?��
�ο��𰸣���1�����ˣ�2�֣�
��2��ȡ������ҺB���Թ��У���������KSCN��Һ������Һ��ɺ�ɫ������ҺB�к���Fe3�� ��2�֣�
��3��SiO2��2�֣�AlO2�D��2H2O��CO2=HCO3�D��Al(OH)3����2�֣�
��4�����ͷ�?����θ�����ȣ�2�֣�
�������������������������е�Al2O3��Fe2O3��MgO�ܺ����ᷴӦ����SiO2�����ܽ⣬��������A��SiO2���������ǹ��ˣ����õ���ҺB���Ȼ������Ȼ������Ȼ�þ�Լ����������ᣬ�����мӹ������ռ���ò�����CΪMg(OH)2? Fe(OH)3��������Ҳ�ǹ��ˣ� ������ҺD����Ҫ�ɷ�Ϊƫ�����ƣ�ͨ�����CO2�Ļ�ѧ����ʽΪNaA1O2+CO2+H2O=Al(OH)3 ��+NaHCO3��������Ҳ�ǹ��ˣ������Ƿ��룬������EΪAl(OH)3�����պ����ɲ���GΪAl2O3����1�������������Ϊ���ˣ��𰸣����ˡ���2����֤��ҺB���Ƿ���Fe3+�ķ�����ȡ������ҺB���Թ��У���������KSCN��Һ������Һ��ɺ�ɫ������ҺB�к���Fe3�� ���𰸣�ȡ������ҺB���Թ��У���������KSCN��Һ������Һ��ɺ�ɫ������ҺB�к���Fe3�� ����3��������A��SiO2��д��D��E��Ӧ�����ӷ���ʽ��AlO2�D��2H2O��CO2=HCO3�D��Al(OH)3�����𰸣�SiO2��2�֣�AlO2�D��2H2O��CO2=HCO3�D��Al(OH)3����2�֣�����4��NaHCO3�������ƴ���������ͷۡ�����θ�����ȣ���;���ͷ�?����θ�����ȡ�
�����Ѷȣ�һ��
4������� ����10�֣����������� �����ռ���CO2��Ȼ����10mLŨNaO
�����ռ���CO2��Ȼ����10mLŨNaO H��Һ��Ѹ���ܷ������ڣ����Թ۲쵽������ͻȻ����ˣ�ԭ���� �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ���Ӧ�����ӷ���ʽΪ �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߡ�
H��Һ��Ѹ���ܷ������ڣ����Թ۲쵽������ͻȻ����ˣ�ԭ���� �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ���Ӧ�����ӷ���ʽΪ �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߡ�
һ��ʱ����ֿ��Թ۲쵽 �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ�
ԭ���� �ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ���Ӧ�Ļ�ѧ����ʽΪ
�ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ� �ߣߣߣߣߣߣߣߣߣߣߡ�
�ߣߣߣߣߣߣߣߣߣߣߡ�
�ο��𰸣�

�����������
�����Ѷȣ�һ��
5��ѡ���� �������ǻ�ѧѧϰ�г��õ�һ��˼ά������������������ȷ����
[? ]
A�����ʶ�����ͬ��Ԫ����ɵģ�ֻ��һ��Ԫ�ص�����һ���Ǵ�����
B�����������ڽ������˳�������Ԫ�ص�ǰ�棬�����ᷴӦһ���ų�����
C���кͷ�Ӧ�����κ�ˮ���ɣ����κ�ˮ���ɵķ�Ӧ�������кͷ�Ӧ
D���������ж�������Ԫ�أ�����Ԫ�صĻ����ﲻһ����������
�ο��𰸣�D
���������
�����Ѷȣ���