1、选择题 常温下,可用铝制容器盛放的是( )
A.浓硝酸
B.稀盐酸
C.稀硝酸
D.NaOH溶液
参考答案:A、在常温下,浓硝酸具有“强氧化性”,可以在铝制器皿表明形成一层致密的氧化物薄膜,阻止酸和金属的继续接触,可以用铝制容器盛装浓硝酸,故A正确;
B、铝与盐酸反应生成氯化铝与氢气,铝被腐蚀,不能用铝制容器盛装盐酸,故B错误;
C、金属铝和稀硝酸反应,铝被腐蚀,不能用铝制容器盛装稀硝酸,故C错误;
D、铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,铝被腐蚀,不能用铝制容器盛装氢氧化钠溶液,故D错误;
故选A.
本题解析:
本题难度:简单
2、选择题 下列物质既能与盐酸反应,又能与烧碱溶液反应的是
①Al2O3 ②Al(OH)3 ③Al ④NaHCO3 ⑤NaHS ⑥CaCO3 ⑦NaHSO4 ⑧NaHSO3
[? ]
A、除⑥外
B、除⑥、⑦、⑧外
C、除⑥、⑦外
D、除①、②、③、④、⑤外
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列各组离子加入足量的氨水后,现象有明显不同的是( )
①Al3+、Fe3+
②Al3+、Cu2+
③K+、Ba2+
④Mg2+、Al3+
⑤Fe3+、Fe2+
A.①②⑤
B.①②④⑤
C.①②④
D.③④⑤
参考答案:A
本题解析:③中均无明显现象,④中均产生白色沉淀。
本题难度:简单
4、选择题 由Al3+→Al(OH)3→AlO2-→□→Al3+系列变化中,□中应填写的是
[? ? ]
A.Al(OH)3
B.AlCl3
C.HCl
D.NaOH
参考答案:A
本题解析:
本题难度:简单
5、实验题 已知甲和I、L、M均为常见的单质,I在常温下为气体,L、M为金属;气体K的水溶液显碱性;A是由前20号元素组成的阴阳离子个数比为1∶1的离子化合物,且阴离子含有14个电子;乙是一种红棕色的粉末,G为白色胶状沉淀,D在常温下是无色液体,C的溶液常用于在实验室检验E。各物质之间的转化关系如下图所示(部分物质在图中没有列出)。

请根据要求填空:
(1)A的化学式为______________________,E的电子式为_______________________。
(2)反应①的化学方程式为___________________________________________________。
(3)反应②的化学方程式为___________________________________________________。
(4)J→G的离子方程式为_____________________________________________________。
参考答案:
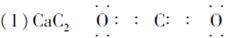
(2)H2O+C CO+H2
CO+H2
(3)2Al+Fe2O3 2Fe+Al2O3
2Fe+Al2O3
(4)CO2+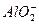 +2H2O====Al(OH)3↓+
+2H2O====Al(OH)3↓+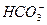 (其他合理答案均可)
(其他合理答案均可)
本题解析:该题的突破口是“乙是一种红棕色的粉末”可知乙是Fe2O3,由L、M为金属单质可知L、M分别为Al、Fe,推出I、J、D分别为H2、NaAlO2、H2O,由G为白色胶状沉淀可知G为Al(OH)3;由气体K的水溶液显碱性可知K为NH3;因为H与Fe2O3反应生成Fe,所以H有还原性,可推出甲、H、E分别为C、CO、CO2,所以B中一定含有C、H两种元素,可能含有O元素;由C的溶液常用于在实验室检验E(CO2)可知C为Ca(OH)2,A为CaC2,B为C2H2,N为铵盐。最后再从头到尾顺一遍。
本题难度:简单