1��ѡ���� ���з�Ӧ������������ԭ��Ӧ���ǣ�?��?
A��CO2+H2O==H2CO3
B��H2CO3==CO2��+H2O
C��CaCO3+2HCl==CaCl2+H2O+CO2��
D��CO2+C����2CO
�ο��𰸣�D
���������
��ȷ�𰸣�D
A��B��C��Ԫ�ػ��ϼ۾����䣬�Ƿ�������ԭ��Ӧ��
�����Ѷȣ���
2��ѡ���� �����йػ�ѧ�����ʾ��ȷ���ǣ�?��
A��Beԭ�ӵĽṹʾ��ͼ��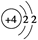
B������Ľṹ��ʽ��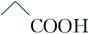
C��������Ϊ16����ԭ�ӣ�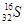
D��NH4Cl�ĵ���ʽ��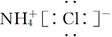
�ο��𰸣�A
���������B�����Ľṹ��ʽΪCH3��COOH�������ж���һ��CH2������C�Ӧ��ʾΪ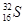 ��D�NH4Cl�ĵ���ʽӦΪ
��D�NH4Cl�ĵ���ʽӦΪ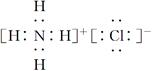 ��
��
�����Ѷȣ�һ��
3��ѡ���� ��ɫ��ѧ�Ǵ�Դͷ�Ϸ�ֹ��Ⱦ������ѧ���̶Ի����ĸ���Ӱ�콵�͵�����ȵĻ�ѧ��������������Ӧ��ѭ��ɫ��ѧ��ԭ��ѧʵ��ҲӦ��ѭ��ɫ��ѧԭ��ʵ��ԭ�Ϻ��̵���ɫ��������ʵ���ʵ�������ѭ��ɫ��ѧԭ�����
A���ö�����������������ʵ��
B����˫��ˮ����������������
C������ˮ�����ˮ������ȡʵ��
D����ͭ�۴���ͭ˿����Cu��ŨHNO3�ķ�Ӧ
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ���ö�����������������ʵ�飬����������ŷŵ������У���Ⱦ����? B����ȷ����˫��ˮ������������������H2O2��Ӧ����������ˮ�� C������ȷ������ˮ�����ˮ������ȡʵ�飬���ӷ���D������ȷ����ͭ�۴���ͭ˿����Cu��ŨHNO3�ķ�Ӧ��ͭ˿�ÿ��Ʒ�Ӧ������ֻҪ��ͭ˿�������ʹ��Ӧֹͣ��
�����Ѷȣ�һ��
4������� 4.35g������������Ũ���ᣨ�ܶ�Ϊ1.19g?cm-3����������Ϊ36.5%����ȫ��Ӧ����
��1��������HCl�����ʵ���Ũ�ȣ�
��2����������HCl�����ʵ�����
��3������������ȫ����ʯ�������գ��ɵõ�Ư�۵�������
�ο��𰸣���1���ܶ�Ϊ1.19g?cm-3����������Ϊ36.5%Ũ��������ʵ���Ũ��Ϊ1000��1.19��36.5%36.5mol/L=11.9mol/L��
��������HCl�����ʵ���Ũ��Ϊ11.9mol/L��
��2��4.35g�������̵����ʵ���Ϊ4.35g87g/mol=0.05mol����
MnO2+4HCl�TMnCl2+Cl2��+2H2O
?1? ? 1
0.05mol? n��Cl2��?
��n��Cl2��=0.05mol
��������HCl����Cl2��������ԭ���غ��֪����������HCl�����ʵ�����Cl2��2����
�ʱ�������HClΪ0.05mol��2=0.1mol��
�𣺱�������HCl�����ʵ�����0.1mol��
��3��n��Cl2��=0.05mol����ʯ�������գ���
2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O
2? 1? 1
0.05mol?n��CaCl2��? ?n[Ca��ClO��2]
����n��CaCl2��=n[Ca��ClO��2]=0.05mol��12=0.025mol��
�ʿɵ�Ư�۵�����Ϊ��0.025mol��111g/mol+0.025mol��143g/mol=6.35g��
������ȫ����ʯ�������գ��ɵõ�Ư�۵�����Ϊ6.35g��
���������
�����Ѷȣ�һ��
5��ѡ���� (NH4)2Cr2O7��һ�������ֽ���Ρ����и����(NH4)2Cr2O7���ȷֽ������жϣ�����ʵ�ʵ���
A��CrO3 + NH3 + H2O
B��Cr2O3 + NH3 + H2O
C��CrO3 + N2 + H2O
D��Cr2O3 + N2+ H2O
�ο��𰸣�D
�����������
�����Ѷȣ�һ��