1������� д���������ʵĵ��뷽��ʽ��
��1��Al2��SO4��______��2��NaHCO3______��
�ο��𰸣���1����������ǿ�����ˮ��Һ����ȫ���룻���������뷽��ʽΪ��Al2��SO4��3=2Al3++3SO42-��
�ʴ�Ϊ��Al2��SO4��3=2Al3++3SO42-��
��2��̼������������ǿ����ʽ�Σ���ǿ�������ȫ���룻���뷽��ʽΪ��NaHCO3=Na++HCO3-��
�ʴ�Ϊ��NaHCO3=Na++HCO3-��
���������
�����Ѷȣ�һ��
2������� NH4Al(SO4)2��ʳƷ�ӹ�����Ϊ��ݵ�ʳƷ���Ӽ������ڱ���ʳƷ�У�NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺����ش��������⣺
��1��NH4Al(SO4)2������ˮ������������ (�ñ�Ҫ�Ļ�ѧ������������˵��)��
��2����ͬ�����£�0��1 mol��L��1NH4Al(SO4)2��c(NH4+) (����ڡ��������ڡ���С�ڡ�)0��1 mol��L��1NH4HSO4��c(NH4+)��
��3��

��ͼ��0��1 mol��L��1�������Һ��pH���¶ȱ仯��ͼ��
�����з���0��1 mol��L��1NH4Al(SO4)2��pH���¶ȱ仯�������� (��д��ĸ)������pH���¶ȱ仯��ԭ���� ��
��20 ��ʱ��0��1 mol��L��1NH4Al(SO4)2��2c(SO42-)��c(NH4+)��3c(Al3��)�� ��
��4������ʱ����100 mL 0��1 mol��L��1NH4HSO4��Һ�еμ�0��1 mol��L��1NaOH��Һ���õ���ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��

�Է���ͼ��a��b��c��d�ĸ��㣬ˮ�ĵ���̶������� ����b�㣬��Һ�и�����Ũ���ɴ�С������˳���� ��
�ο��𰸣���1��Al3��ˮ�����ɵ�Al(OH)3������������ԣ���Al3����3H2O Al(OH)3(����)��3H����Al(OH)3����������������ʹ������Ӷ�����ˮ��(2��)
Al(OH)3(����)��3H����Al(OH)3����������������ʹ������Ӷ�����ˮ��(2��)
��2����
��3���٢�NH4Al(SO4)2ˮ�⣬��Һ�����ԣ������¶���ˮ��̶�����pH��С ��10��3mol��L��1
��4��a (Na��)>c(SO42-)>c(NH4+>c(OH��)��c(H��)
�����������1������ NH4Al(SO4)2����ˮ�������Al3��ˮ�����ɵ�Al(OH)3������������ԣ���Al3����3H2O Al(OH)3��3H����Al(OH)3������������ʹ������Ӷ�����ˮ��
Al(OH)3��3H����Al(OH)3������������ʹ������Ӷ�����ˮ��
��2������NH4HSO4����ˮ��ȫ����������ӣ�����NH4��ˮ�⣬������ͬ�����£�0��1 mol��L��1NH4Al(SO4)2��c(NH4��)С��0��1 mol��L��1NH4HSO4��c(NH4��)��
��3�������� NH4Al(SO4)2����ˮ�������NH4����Al3��ˮ����Һ�����ԣ���ˮ�������ȵģ�����ٽ�ˮ�⣬��Һ��������ǿ��pH��С����˷���������������I��
��20 ��ʱ��0��1 mol��L��1NH4Al(SO4)2��pH��3�����ݵ���غ��֪��20 ��ʱ��0��1 mol��L��1NH4Al(SO4)2��2c(SO42��)��c(OH��) ��c(NH4��)��c(H��)��3c(Al3��)���� 2c(SO42��)��c(NH4��)��3c(Al3��)��c(H��)��c(OH��) ��10��3-10��11mol��L��1��
��4����100 mL 0��1 mol��L��1 NH4HSO4��Һ�еμ�0��1 mol��L��1 NaOH��Һ��Ӧ�����ӷ���ʽ���ΪH����OH��=H2O��OH����NH4��=NH3��H2O��d��ǡ���к������ӣ���Һ�е�NH4��ˮ��ٽ�ˮ�ĵ��롣D��֮��NH4��Ũ�ȼ�С��������Һ��ˮ�ĵ���̶������a�㣻��b�㣬pH��7����Һ�����ԣ���Һ�е������������ƺ�����狀Ͱ���������Һ�и�����Ũ���ɴ�С������˳����c(Na��)��c(SO42��)��c(NH4��)��c(OH��)��c(H��)��
���㣺���齺�����ʡ�ˮ�ĵ��롢����ˮ�⡢��Һ������Ũ�ȴ�С�Ƚϡ�
�����Ѷȣ�����
3��ʵ���� ��17�֣����ᾧ�����ɿɱ�ʾΪH2C2O4��xH2O��ʵ���ҳ�������ȷֽ���ȡCO���壬��Ӧ����ʽΪ��H2C2O4��xH2O  CO+CO2+(x+1)H2O����ͼΪ�ֽ���ᾧ�壬�ø��﴿����CO��ԭCuO��ȡCu�����ռ�CO��ʵ��װ��(��ȥ����̨�����е�֧�żӳ�װ��)���ش��������⡣
CO+CO2+(x+1)H2O����ͼΪ�ֽ���ᾧ�壬�ø��﴿����CO��ԭCuO��ȡCu�����ռ�CO��ʵ��װ��(��ȥ����̨�����е�֧�żӳ�װ��)���ش��������⡣

��1��Aװ��Ϊ���ȷֽ�����װ�ã���װ�ô�����_________________��Cװ����ʢ�ŵ��Լ���_______ (�ѧʽ)��Eװ�õ�������__________��
��2��ʵ��������漰�����²�����
�ٵ�ȼA���ľƾ���
��Ϩ��A���ľƾ���
�۵�ȼD���ľƾ���
��Ϩ��D���ľƾ��ơ�
��4���������ȵ����˳��Ϊ_______(�����)����ȼD���ƾ���ǰ����Ҫ���еIJ���������__________��
��3�������Ը��������Һ�ζ����ᾧ�壬��x��ֵ��
ʵ�鲽�裺ȷ��ȡ1.17g ���ᾧ�壬���100mL��Һ��ȡ��20.00mL����ƿ�У�����ƿ�м�������ϡH2SO4����0.0500mol/L���Ը��������Һ�ζ����ζ����յ�ʱ���ĸ��������Һ16.00mL���ζ�ʱ���������ķ�ӦΪ��2MnO4��+5H2C2O4+6H+ = 10CO2+2Mn2++8H2O��
�����Ʋ�����Һ����Ҫ���������ձ�����һ����Ҫ�IJ���������_____________��
��x=________��
��4��Ϊ̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죬�ڼ����Թ��зֱ������������
�Թ�
| 0.01mol/L KMnO4
| 0.1mol/L H2C2O4
| 0.1mol/L H2SO4
| MnSO4����
|
��
| 4 mL
| x mL
| 1 mL
| ��
|
��
| y mL
| 2mL
| 1 mL
| ��
|
��x=_______��y=________���ܹ��ó������Ը÷�Ӧ��Ӱ����۵�ʵ��������___________________��
�ο��𰸣���1���Թܿ�Ӧ������б(��Ӧ������б)��Ũ���ᣬ��ȫƿ(�������)
��2���٢ۢܢڣ��鴿
��3����100mL����ƿ����ͷ�ιܣ� ��1.5
��4��2��4������MnSO4������Թ�����Һ��ɫ���ʱ�δ�ӵĿ졣
�����������1����ͼ��֪������ʱ���Թܿ�Ӧ��������б���������ɵIJ���ΪCO��CO2��H2O��B�м�������CO2�����ʣ�C�м���Ũ������и��EΪ��ȫƿ����ֹҺ�嵹����
��2����ʵ������У�Ӧ�ȵ�ȼA���ľƾ��ƣ��ٵ�ȼD���ľƾ��ƣ���Ӧ���������෴����Ϩ��D���ľƾ��ƣ���Ϩ��A���ľƾ��ƣ�ʵ��������õ�����CO��Ϊ��ȼ�ױ������壬����Ҫ��ʹ��ǰ�鴿��
��3����ʵ��������һ��Ũ�ȵ���Һ����Ҫ��������������ƽ���ձ���������������ƿ����ͷ�ιܵȣ��������ڲ����������Dz��������ձ���100ml����ƿ����ͷ�ιܣ�
��2MnO4-~5H2C2O4
25
0.0008mol0.002mol
n(H2C2O4)=0.002��5=0.01mol
����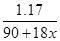 =0.01���x=1.5
=0.01���x=1.5
��4���������֪���Աȴ����Ĵ�Ч������ô������������ͬ�������±Ƚϣ���x=2��y=4��ͨ������ó����ۼ���MnSO4������Թ�����Һ��ɫ���ʱ�δ�ӵĿ졣
���㣺ʵ����������ۣ���ѧ��Ӧ�Ļ������㣬�����Ĵ�Ч���ıȽ�
�����Ѷȣ�����
4������� ����һ�仰������������ֵ��ǰ��ΪM������ΪN��M��N�Ĺ�ϵ��A��B��C��D ��ѡ��
A��M>N B��M<N C�� M="N" D�� ���Ƚ�
��1����ͬ�¶��£�1L 1mol/L ��NH4Cl��Һ��2 L 0.5mol��L��1NH4Cl��Һ������Һ��NH4+�ĸ����� ��
��2����ͬ�¶��£�pHֵΪ12���ռ���Һ��CH3COONa��Һ������Һ��ˮ�ĵ���̶ȣ� ��
��3�����������ݵ�Ũ�ȵĴ�����Һ�����ڶ��������¶ȣ�����Һ��c(HCO3��)�� ��
��4����pHֵΪ2�Ĵ�������ᶼϡ����ͬ��������ϡ��Һ��pHֵ�� ��
�ο��𰸣���1��A ��2��B ��3��B ��4��B
�����������1���Ȼ���У�笠�����ˮ�⣬笠�����Ũ��Խ��ˮ��̶�ԽС������ͬ�¶��£�1L 1mol/L ��NH4Cl��Һ�е�NH4+��������2L 0.5mol?L-1NH4Cl��Һ��NH4+�ĸ������ʴ�Ϊ��A����2��pHֵΪ12���ռ���Һ��ˮ�������������Ũ��Ϊ10-12mol/L��pHֵΪ12��CH3COONa��Һ��ˮ�������������Ũ��Ϊ10-2mool/L��������ͬ�¶��£�pHֵΪ12���ռ���Һ��ˮ�ĵ����С��pHֵΪ12��CH3COONa��Һ��ˮ�ĵ���ȣ��ʴ�Ϊ��B����3��̼������Һ�У�̼�����ˮ��̶������¶ȵ����߶����������¶��Ի��ң�̼�������Ũ�����ʴ�Ϊ��B����4�����������ᣬϡ�ʹٽ����룬������ǿ�ᣬϡ����Ũ�ȼ�С�����Խ�pHֵΪ2�Ĵ�������ᶼϡ����ͬ��������ϡ��Һ��pHֵ�Ǵ����С������ģ��ʴ�Ϊ��B��
���㣺Ӱ������ˮ��̶ȵ���Ҫ���أ��й�ph�ļ���
�����Ѷȣ�һ��
5��ѡ���� ���е��뷽��ʽ��д��ȷ���ǣ�������
A��CaCl2�TCa2++2Cl-
B��K2CO3�TK2++CO32-
C��Ba��OH��2�TBa2++��OH��2-
D��FeCl3�TFe2++3Cl-
�ο��𰸣�A
���������
�����Ѷȣ���