|
|
|
高考化学必考知识点《水的电离平衡》在线测试(2019年最新版)(七)
2019-07-03 23:51:15
【 大 中 小】
|
1、实验题 (13分)使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到___________(填仪器名称)中定容,摇匀即得。
(2)用 取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴 作指示剂。
(3)读取盛装0.1000 mol/L NaOH 溶液的 (填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为 mL。
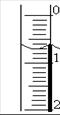
(4)滴定。当 时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数
实验数据(mL)
| 1
| 2
| 3
| 4
| V(样品)
| 20.00
| 20.00
| 20.00
| 20.00
| V(NaOH)(消耗)
| 15.95
| 15.00
| 15.05
| 14.95
|
Ⅲ.数据处理与讨论:
(1)经计算,市售白醋总酸量= g/100mL。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是 (填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
2、选择题 室温下,某无色透明溶液中由水电离出来的H+和OH―浓度的乘积为1×10―24,则此溶液中可能大量共存的离子组为( )
A.HCO3-、Al3+、Na+、SO42-
B.I-、NO3-、K+、NH4+
C.MnO4-、Cl-、SO42-、K+
D.SiO32-、SO32-、Na+、Cl-
|
3、选择题 下列说法正确的是
A.40℃时,0.005 mol・L-1 H2SO4溶液的pH为2
B.往氯化铁溶液中滴加氨水来制备氢氧化铁胶体
C.镀锌铁制品镀层受损后,铁制品易生锈
D.已知NaCl溶液和CH3COONH4溶液均显中性,则两溶液中水的电离程度相同
|
4、选择题 将pH=5的盐酸溶液稀释1000倍后,溶液的pH为
A.等于8
B.等于7
C.略小于7
D.略大于7
5、选择题 已知在常温下溶液中的pH+pOH=14,又已知正常人(人的体温高于室温)血液的pH=7.3,则正常人血液的pOH是
A.大于6.7
B.小于6.7
C.等于6.7
D.无法判断