1、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是(? )
A.11.2 L N2所含分子数为0.5NA
B.常温下,16 g CH4中共用电子对的数目为4NA
C.一定温度下,1 mol FeCl3水解生成NA个Fe(OH)3胶体颗粒
D.在反应H2O2+Cl2=2HCl+O2中,每生成32 g氧气,转移4NA个电子
参考答案:B
本题解析:未指明温度和压强,一定体积气体的物质的量不能确定,A项错误;1个CH4分子中含有4个共用电子对,16 g CH4中含有共用电子对的数目为4NA,B项正确;由于Fe(OH)3胶体粒子是由若干个Fe(OH)3分子聚集而成的微粒集体,因此1 mol FeCl3水解为胶体后,胶体粒子数小于NA,C项错误;在反应H2O2+Cl2=2HCl+O2中,每生成32 g氧气,转移2NA个电子,D项错误。
本题难度:一般
2、选择题 下列溶液中溶质的物质的量浓度为1 mol・L-1的是(? )
A.将40 g NaOH溶解于1 L水中配成的NaOH溶液
B.常温常压下将22.4 L HCl 气体溶于水配成1 L的盐酸溶液
C.将1 L 10 mol/L的浓盐酸与9L水混合配成溶液
D.从1000 mL 1 mol/L NaCl溶液中取出100 mL的溶液
参考答案:D
本题解析:A选项40gNaOH为1molNaOH但溶于一升水中不知最终溶液的体积c(物质的量浓度)=溶剂物质的量/溶液的体积故A不正确B选项是常温常压下只有在标准状况下22.4LHCL=1mol的HCL标况下盐酸溶液的物质的量浓度才为1mol/L ? C选项仍不知混合后的溶液体积D选项取1mol/LNaCl的溶液任意毫升浓度不变故D正确
本题难度:简单
3、选择题 往含0.2molKOH和0.1molCa(OH)2的溶液中持续地通入CO2气体,当通入气体的体积为6.72L(标准状况)时立即停止,则在这一过程中,溶液中离子的物质的量n和通 入CO2的体积V的关系示意图正确的是(气体的溶解和离子的水解忽略)?
入CO2的体积V的关系示意图正确的是(气体的溶解和离子的水解忽略)?
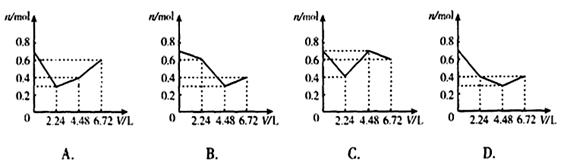
参考答案:D
本题解析:略
本题难度:简单
4、选择题 下列叙述中正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol
D.2H既可以表示2个氢原子又可以表示2mol氢原子
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列说法正确的是
A.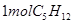 分子中,含
分子中,含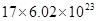 个共用电子对
个共用电子对
B.在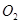 参与的反应中,
参与的反应中,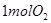 作氧化剂时,得到电子数一定是
作氧化剂时,得到电子数一定是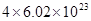
C.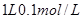 的
的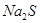 溶液中硫离子数为
溶液中硫离子数为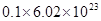
D.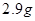 乙基(
乙基(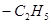 )含有的电子数为
)含有的电子数为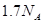
参考答案:D
本题解析:略
本题难度:简单