1、选择题 若20 g密度为ρ g・cm-3的Ca(NO3)2溶液里含1 g Ca2+,则NO-3的浓度是(? )
A. mol・L-1
mol・L-1
B. mol・L-1
mol・L-1
C.2.5ρ mol・L-1
D.1.25ρ mol・L-1
参考答案:C
本题解析:根据溶液中电荷守恒,可得下式:
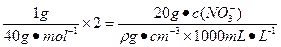
c(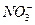 )="2.5ρ" mol・L-1
)="2.5ρ" mol・L-1
本题难度 :简单
2、选择题 下列说法正确的是(? )
A.摩尔是物理量之一
B.某物质含有6.02×1023个粒子,这种物质的物质的量就是1 mol
C.1 mol氧
D.1 mol KClO3和1 mol SO2中,所含氧原子的个数比为3∶2
参考答案:D
本题解析:本题考查对物质的量基本概念的掌握情况。
对于A选项,摩尔是物质的量的单位,不是物理量;对于B选项,物质的量研究的对象是粒子,即含阿伏加德罗常数个粒子才是1 mol,而不是一定量的物质是1 mol。如0.5 mol H2中就含有6.02×1023个氢原子,但氢气的物质的量却是0.5 mol;C选项中未指明粒子的种类;D选项1 mol KClO3中含氧原子3 mol,1 mol SO2中含氧原子2 mol,由N="n" NA可知两粒子的个数比等于其物质的量之比,故D项正确。
本题难度:简单
3、实验题 用18mol/L 浓硫酸配制100 mL 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 转移、洗涤 ⑤ 定容、摇匀
回答下列问题
(1)所需浓硫酸的体积是_________,量取浓硫酸所用的量筒的规格是_________
(从下列中选用 A. 10ml B. 20ml C. 50ml D. 100ml)
(2)第③步实验的操作是_________。
(3)第⑤步实验的操作所用到的仪器有_________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A. 所用的浓硫酸长时间放置在密封不好的容器中_________
B. 容量瓶用蒸馏洗涤后残留有少量的水_________
C. 所用过的烧杯、玻璃棒未洗涤_________
D. 定容时俯视溶液的液凹面_________
参考答案:(1)16.7mL;B. 20mL
(2)取一烧杯,先加入适量水,再将量好的浓硫酸延烧杯内壁慢慢注入水中,并用玻璃棒不断搅拌
(3)容量瓶、胶头滴管
(4)A. 偏小;B. 无影响;C. 偏小;D. 偏大
本题解析:
本题难度:一般
4、选择题 设NA表示阿伏加德罗常数的值,下列叙述中正确的是:
A.含4.8g 碳元素的石墨晶体中的共价键数是0.8NA
B.标准状况下,11.2LCO和N2的混合气体中,含有的原子数为NA
C.1mol的羟基(-OH)与1mol的氢氧根离子(OH-)所含电子数均为9NA
D.常压、500℃、催化条件下,1molSO2和0.5molO2充入一密闭容器内,充分反应后的生成物分子数为NA