|
|
|
高中化学知识点归纳《物质的量》试题特训(2019年最新版)(二)
2019-07-03 23:59:23
【 大 中 小】
|
1、选择题 设NA表示阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,22.4LCH4和CH2Cl2的混合物所含有的分子数目为NA
B.3g的甲基中含有的电子数为1.6NA
C.0.5mol的有机物C15H32中含有的共键数为24NA
D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
|
参考答案:D
本题解析:A.不正确,标准状况下, CH2Cl2是液态;
B.不正确,3g的甲基中含有的电子数为2NA ;
C.不正确,烷烃中共价键的数目,碳原子的3倍加强,0.5mol的有机物C15H32中含有的共键数为23NA
D.正确;选D。
本题难度:一般
2、选择题 下列叙述正确的是(?)
A.摩尔是物质的数量单位
B.1mol氧气的质量是32 g・mol-1。
C.CO2的摩尔质量是44g
D.0.5 mol H2SO4中含有2mol氧原子
参考答案:D
本题解析:略
本题难度:简单
3、实验题 实验室需要480 mL 0.4 mol・L-1 的NaCl溶液,有如下操作步骤:
①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解
②把①所得溶液小心转入一定容积的容量瓶中
③继续向容量瓶中加蒸馏水至液面距刻度线1 cm~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶瓶塞塞紧,充分摇匀
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)_______________。
(2)实验室有如下规格的容量瓶:①100 mL,②250 mL,③500 mL,④1 000 mL,本实验选用________。
(3)本实验用到的基本实验仪器除容量瓶、玻璃棒外还有:_________________。
(4)需要使用玻璃棒的操作有________(填序号),其作用为_________________。
(5)误差分析:(填“偏高”、“偏低”或“无影响”)
①称量NaCl时,物码倒置(1g以下用游码)________。
②某同学观察液面的情况如图所示,对所配溶液浓度将有何影响?________。
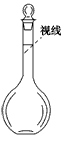
③没有进行操作步骤④________
④加蒸馏水时不慎超过了刻度线,立即用胶头滴管将多余的水吸出__________
⑤容量瓶原来有少量水___________
参考答案:(1)①②④③⑤
(2)③
(3)天平、药匙、烧杯、胶头滴管、量筒
(4)①②③④;①:搅拌,促进溶解、②③④:引流
(5)①偏低;②偏高;③偏低;④偏低;⑤无影响
本题解析:
本题难度:一般
4、选择题 下列叙述正确的是(?)
A.2 mol NaOH的摩尔质量为80g/mol
B.NH4+的摩尔质量为17 g/mol
C.常温常压下,32g SO2含有的分子数约为3.01×1023
D.2mol/L的CaCl2溶液中Cl-的数目为2NA
参考答案:C
本题解析:略
本题难度:简单
5、填空题 在120 ℃时分别进行如下四个反应:
A.2H2S+O2====2H2O+S
B.2H2S+3O2====2H2O+2SO2
C.C2H4+3O2====2H2O+2SO2
D.C4H8+6O2====4H2O+4CO2
|
(1)若反应在容积固定的容器内进行,反应前后气体密度(d)和气体总压强(p)分别符合关系式d前=d后和p前>p后的是_________;符合关系式d前=d后和p前=p后的是_________。(请填写反应的代号)
(2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系d前>d后和V前<V后的是_________;符合d前>d后和V前>V后的是_________。(请填写反应的代号)
参考答案:(1)B? C? (2)D? A
本题解析:(1)因是固定的容器,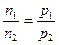 ,反应B是5 mol气体,反应后生成4 mol气体(H2O在120 ℃时是气体),所以p前>p后;反应C是4 mol气体,反应后生成4 mol气体,p前=p后。
,反应B是5 mol气体,反应后生成4 mol气体(H2O在120 ℃时是气体),所以p前>p后;反应C是4 mol气体,反应后生成4 mol气体,p前=p后。
(2)在同压时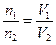 ,反应D是7 mol气体,反应生成8 mol气体,V前<V后,也符合d前>d后,反应A由于生成了固体S,其d前>d后,而且生成的气体物质的量减少,体积减少,即V前>V后。
,反应D是7 mol气体,反应生成8 mol气体,V前<V后,也符合d前>d后,反应A由于生成了固体S,其d前>d后,而且生成的气体物质的量减少,体积减少,即V前>V后。
本题难度:简单
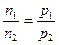 ,反应B是5 mol气体,反应后生成4 mol气体(H2O在120 ℃时是气体),所以p前>p后;反应C是4 mol气体,反应后生成4 mol气体,p前=p后。
,反应B是5 mol气体,反应后生成4 mol气体(H2O在120 ℃时是气体),所以p前>p后;反应C是4 mol气体,反应后生成4 mol气体,p前=p后。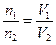 ,反应D是7 mol气体,反应生成8 mol气体,V前<V后,也符合d前>d后,反应A由于生成了固体S,其d前>d后,而且生成的气体物质的量减少,体积减少,即V前>V后。
,反应D是7 mol气体,反应生成8 mol气体,V前<V后,也符合d前>d后,反应A由于生成了固体S,其d前>d后,而且生成的气体物质的量减少,体积减少,即V前>V后。