1、实验题 运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高。下列措施不能够有效控制CO2所导致的温室效应的是_________(填序号)
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出84消毒液露置在空气中发生反应的离子方程式___________________________。
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。
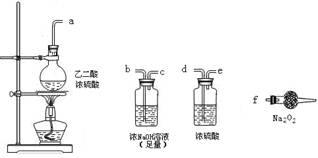
已知: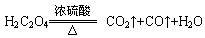 ,则实验选择的最简单的装置接口连接顺序为________;
,则实验选择的最简单的装置接口连接顺序为________;
若CO能够与Na2O2发生反应,则预测反应产物为____________。实验后用球形干燥管中的固体进行验证可选择的试剂是_______________________________。
(4)已知C(s)+O2(g)=CO2(g),△H="-393.5" kJ・mol -1 ;CO(g)+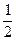 O2(g)=CO2(g),△H="-283.0" kJ・mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
O2(g)=CO2(g),△H="-283.0" kJ・mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
参考答案:
(1)④(1分)
(2)ClO-+CO2+H2O=HClO+HCO3-(2分)? 2HClO====2H++2Cl-+O2↑(2分)
(3)abcf(1分)? Na2CO3(1分)
稀H2SO4和澄清石灰水或CaCl2溶液(2分)
(4)CO2 (g)+C(s)=" 2CO(g)?" △H="+172.5" kJ・mol -1?(2分)
CO+ CO32-→2CO2+2e-?(2分)?11.2 (2分)
本题解析:略
本题难度:简单
2、选择题
A.它是一种离子化合物
B.它是一种新型化合物
C.它是一种硅酸盐
D.它是由两种单质组成的混合物
参考答案:B
本题解析:形成化合物的两种元素间只有共价键,故应为共价化合物,故ACD不正确,B正确;
本题难度:一般
3、计算题 (1)钾玻璃中含有18.4%的K2O,11.0%的CaO和70.6%的SiO2,试计算这三种氧化物的物质的量之比。?
(2)若需制造5.10 t钾玻璃,需用K2CO3、CaCO3和SiO2各多少吨??
(3)写出制钾玻璃的化学方程式及钾玻璃的主要成分。?
参考答案:(1)1∶1∶6
(2)1.38 t、1.00 t、2.72 t
(3)K2CO3+SiO2 K2SiO3+CO2↑,CaCO3+SiO2
K2SiO3+CO2↑,CaCO3+SiO2 CaSiO3+CO2↑。
CaSiO3+CO2↑。
钾玻璃的主要成分是CaSiO3、K2SiO3和SiO2。
本题解析:(1)?n?(K2O)∶?n?(CaO)∶?n?(SiO2)=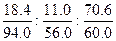 ?=0.196∶0.196∶1.18 = 1∶1∶6
?=0.196∶0.196∶1.18 = 1∶1∶6
可见该钾玻璃的化学式为K2O・CaO・6SiO2或K2SiO3・CaSiO3・4SiO2,其摩尔质量M="510" g・ mol-1。
(2)5.10 t钾玻璃物质的量为
?n=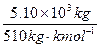 ="10.0" kmol
="10.0" kmol
则m(K2CO3)="138" kg・kmol-1×10.0 kmol="1.38" t(钾原子守恒)
?m(CaCO3)="100" kg・kmol-1×10.0 kmol="1.00" t (钙原子守恒)
?m(SiO2)="5.10" t-1.38 t-1.00 t="2.72" t
(3)与钠玻璃的制法相似,制钾玻璃需要以碳酸钾、石灰石和石英为原料,高温融制。与钠玻璃的成分类似,钾玻璃的主要成分是CaSiO3、K2SiO3和SiO2。
本题难度:简单
4、选择题 将CO2通入下列物质的溶液中,不与其反应的是
①Na2CO3?②Na2SiO3?③Na[Al(OH)4]?④C6H5ONa?⑤Ca(ClO)2?⑥CaCl2?⑦CaCO3
?
A.①③④⑤⑥
B.①和⑥
C.只有①
D.只有⑥
参考答案:D
本题解析:略
本题难度:一般
5、选择题 据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可制备出超高强度的高性能混凝土。下列关于二氧化硅的说法中,正确的是(? )
A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物
B.将二氧化碳通入硅酸钠溶液可以得到硅酸
C.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强
D.二氧化硅是酸性氧化物,它不溶于任何酸
参考答案:B
本题解析:二氧化硅是酸性氧化物,但是二氧化硅不溶于水,不能和水反应生成硅酸,A错误;碳酸的酸性比硅酸强,B正确;该反应是在非溶液状态下进行的反应,属于用不挥发性的酸酐来制取挥发性的酸酐,所以二氧化硅在高温下与碳酸钠的反应不能作为判断硅酸与碳酸酸性强弱的依据,C错误;二氧化硅可以与氢氟酸发生反应,D错误。
本题难度:简单