1、选择题 取一定量的NaOH溶液通入CO2后,再继续向该溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,下列有关说法正确的是(?)

A.原溶液中NaOH的物质的量为0.75 mol
B.通入CO2后所得的溶液溶质成分为NaOH和Na2CO3
C.通入CO2后所得的溶液中含有2.5×10-3 mol NaHCO3
D.纵坐标中a的数值为224
参考答案:C
本题解析:由于盐酸逐滴滴入到碳酸盐中的反应为:Na2CO3+HCl NaHCO3+NaCl;NaHCO3+HCl
NaHCO3+NaCl;NaHCO3+HCl NaCl+CO2↑+H2O,从图像中分析可以发现0~25 mL段消耗的酸体积小于生成气体的体积段消耗酸的体积,所以可以得到溶质的成分是NaHCO3和Na2CO3的混合物,且根据0~25 mL段消耗酸的体积可以判断出Na2CO3的物质的量为2.5×10-3 mol,由25~75 mL段知消耗酸25 mL时,NaHCO3总共(75-25)×10-4 mol=5×10-3 mol,其中由Na2CO3转化过来的NaHCO3是:2.5×10-3 mol,则通入CO2后所得溶液中NaHCO3为:5×10-3 mol-2.5×10-3 mol=2.5×10-3 mol,C正确;其中纵坐标a的数值为112。
NaCl+CO2↑+H2O,从图像中分析可以发现0~25 mL段消耗的酸体积小于生成气体的体积段消耗酸的体积,所以可以得到溶质的成分是NaHCO3和Na2CO3的混合物,且根据0~25 mL段消耗酸的体积可以判断出Na2CO3的物质的量为2.5×10-3 mol,由25~75 mL段知消耗酸25 mL时,NaHCO3总共(75-25)×10-4 mol=5×10-3 mol,其中由Na2CO3转化过来的NaHCO3是:2.5×10-3 mol,则通入CO2后所得溶液中NaHCO3为:5×10-3 mol-2.5×10-3 mol=2.5×10-3 mol,C正确;其中纵坐标a的数值为112。
本题难度:一般
2、选择题 下列说法不正确的有(?)
A.硅酸盐工业使用的每一种原料中都必须含有硅
B.水泥、普通玻璃都是混合物
C.生产水泥、玻璃都需用石灰石
D.用纯净的石英可制成石英玻璃,它的膨胀系数小,常用来制造耐高温的化学仪器
参考答案:A
本题解析:硅酸盐工业中,是大多主要原料为硅酸盐,而不是所有,比如水泥工业, 其中包含一些碳酸钙和石膏这些物质,所以A错误。
本题难度:简单
3、计算题 普通玻璃中,Na2SiO3、CaSiO3、SiO2的物质的量之比是Na2SiO3∶CaSiO3∶SiO2=1∶1∶4。
(1)若以aNa2O・bCaO・mSiO2形式表示此玻璃的组成,则a∶b∶m=____________。
(2)若要制备1 000 kg上述玻璃,需要原料各多少千克?共可产生标准状况下的CO2气体多少升?
参考答案:(1)1∶1∶6
(2)Na2CO3:221.8 kg;CaCO3:209.2 kg;SiO2∶753.1 kg;CO2:9.37×104 L
本题解析:(1)根据原子个数相等的原则,Na2SiO3∶CaSiO3∶4SiO2等同于Na2O・CaO・6SiO2,即a∶b∶m=1∶1∶6.
(2)制造玻璃 的原料是Na2CO3、CaCO3和SiO2,根据反应原理:Na2CO3+SiO2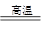 Na2SiO3+CO2↑,CaCO3+SiO2
Na2SiO3+CO2↑,CaCO3+SiO2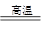 ?CaSiO3+CO2↑。玻璃的化学式为Na2O・CaO・6SiO2,由元素守恒可得关系式:Na2O・CaO・6SiO2→Na2CO3→CaCO3→6SiO2→2CO2。据此可计算出所需的原料和放出CO2的体积。另外还可以用制造1 000 kg玻璃所需的原料和1 000 kg玻璃的差值计算出CO2的质量,继而计算其体积。
?CaSiO3+CO2↑。玻璃的化学式为Na2O・CaO・6SiO2,由元素守恒可得关系式:Na2O・CaO・6SiO2→Na2CO3→CaCO3→6SiO2→2CO2。据此可计算出所需的原料和放出CO2的体积。另外还可以用制造1 000 kg玻璃所需的原料和1 000 kg玻璃的差值计算出CO2的质量,继而计算其体积。
本题难度:一般
4、选择题 两个原硅酸分子的OH原子团之间可以相互作用而脱去一分子水:
2H4SiO4===H6Si2O7+H2O,原硅酸结构为:?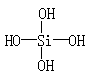 , 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为(?)?
, 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为(?)?
A.5
B.6
C.7
D.8
参考答案:D
本题解析:此题是一道选择题,也是一道信息迁移题。给出的新情境是原硅酸结构及脱水反应,考查内容是H6Si2O7分子中的硅氧键数目。两个原硅酸共有8个硅氧键,当它们相互作用时,虽然有一个硅氧键断裂,但又形成一个新的硅氧键,如图所示:
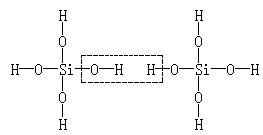
故硅氧键的总数目没有变,仍然是8个。
本题难度:简单
5、选择题 硅是无机非金属材料的主角,下列关于硅及其化合物的说法正确的是(?)
A.硅在自然界中只以化合态的形式存在
B.单质硅常用作半导体材料和光导纤维
C.硅的气态氢化物比甲烷稳定
D.可用石英制造耐酸容器因为二氧化硅不与任何酸反应
参考答案:A
本题解析:略
本题难度:简单