1、填空题 Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁.硫酸亚铁晶体(FeSO4?7H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量.实验步骤如下:
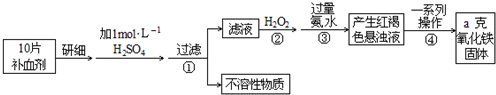
请回答下列问题:
(1)步骤②加入过量H2O2的目的:______;
(2)步骤③中反应的离子方程式:______;
(3)步骤④中一系列处理的操作步骤:______、洗涤、______、冷却、称量.
(4)实验中用浓硫酸配制1mol/L的稀硫酸,配制时用到定量的玻璃仪器有______、______(答出两个仪器).
(5)若实验无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示).
参考答案:(1)双氧水具有氧化性,酸性条件下能将Fe2+全部氧化为Fe3+,故答案为:将Fe2+全部氧化为Fe3+;
(2)步骤③是将Fe3+转化为氢氧化铁沉淀,反应离子方程式为Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,
故答案为:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
(3)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量,
故答案为:过滤;灼烧;
(4)配制一定体积的1mol/L的稀硫酸,配制时需要的仪器有玻棒、烧杯、胶头滴管、容量瓶、量筒,故答案为:容量瓶;量筒;
(5)ag氧化铁中铁元素的质量即为10片补血剂中铁的质量,所以每片补血剂含铁元素的质量ag×11216010=0.07ag,
故答案为:0.07a.
本题解析:
本题难度:一般
2、实验题 为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中。请填空
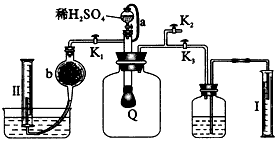
(1)Q内发生反应生成_________种气体,其中的反应有_________个氧化还原反应。
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)_________,打开
_________。
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是_________ 。
(4)导管a的作用是_________。
(5)b中装的固体试剂是_________,为何要缓缓打开K1_________。
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是_________(体积折算到标准状况)。
参考答案:(1)2;1
(2)K1、K2;K3
(3)气球Q慢慢缩小
(4)平衡分液漏斗上下的压强使顺利流下
(5)碱石灰;控制气体流速,使CO2充分吸收
(6)78y/(53x+25y)
本题解析:
本题难度:困难
3、实验题 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是____________________________。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.2H2(g)+O2(g)=2H2O(1) △H<0
C.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式为__________________________________。
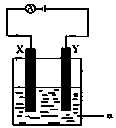
(3)?电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与右图中电解池相连,其中a为电解液, X和Y均为惰性电极,则:
①若a为CuSO4溶液,则电解时的化学反应方程式为 ____________________________________。
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672 mL(标准状况下)时,溶液的pH = __________(假设电解后溶液体积不变)。
参考答案:(1)B
(2)O2 + 4e- + 2 H2O == 4OH-
(3)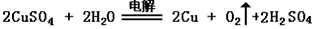
(4)1
本题解析:
本题难度:一般
4、选择题 下列实验方案中,可以测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
①取a克混合物与足量稀盐酸充分反应,取产生的气体体积bmL(折算为标况)
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物充分加热,减重b克?
[? ]
A.?只有①②?
B.?只有②③?
C.?只有③?
D.?全部可以
参考答案:D
本题解析:
本题难度:一般
5、实验题 黄铜矿是工业炼铜的主要原料,主要成分为CuFeS2,含少量脉石。为测定该黄铜矿的纯度,某同学设计了如下实验:

现用电子天平称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和
SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准碘溶液20.00mL。请回答下列问题:
(1)将样品研细后再进行反应,其目的是____________;标准碘溶液应盛放在_______(填“碱式”或“酸式”)?滴定管中。
(2)装置a的作用是_____________。
A.除去空气中的二氧化碳?B.除去空气中的水蒸气 ?
C.有利于气体混合?D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果________(填“偏低”、“偏高”或“无影响”),写出影响测定结果的化学方程式?____________________。
(4)上述反应结束后,仍需通一段时间的空气,其目的是___________________。
(5)通过计算可知,该黄铜矿的纯度为_____________。
(6)假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有___________。
参考答案:(1)使原料充分反应、加快反应速率;酸式
(2)BD
(3)偏低;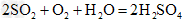
(4)使反应生成的SO2全部进入?d装置中,使测定结果精确
(5)?80%
(6)用水吸收二氧化硫不充分,亚硫酸部分被氧化
本题解析:
本题难度:一般