|
高考化学知识点总结《电解池原理》高频试题预测(2019年最新版)(四)
2019-07-04 00:09:01
【 大 中 小】
|
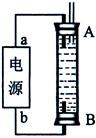
1、选择题 右图为直流电源电解稀Na2SO4溶液的装置。通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液。则下列有关说法中正确的是( )
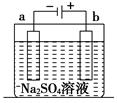
A.a电极产生H2
B.两极产生的气体均有刺激性气味
C.通电一段时间后,稀Na2SO4溶液酸性增强
D.a电极附近呈无色,b电极附近呈红色
|
参考答案:A
本题解析:A、电解硫酸钠溶液,a与电源的负极相连是电解池的阴极,阴极上是阳离子放电,根据离子放电顺序,氢离子放电生成氢气,正确;B、b极是电解池的阳极,氢氧根离子放电,产生氧气,氢气和氧气都不是刺激性气体,错误;C、硫酸钠溶液呈中性,电解的实质是电解水,所以硫酸钠溶液的pH不变,仍是中性溶液,错误;D、a极是氢离子放电,所以氢氧根离子浓度增大,则a极附近呈红色,错误,答案选A。
考点:考查电解中离子的放电顺序的判断,电极产物的判断,电解后溶液的酸碱性的判断
本题难度:一般
2、选择题 如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是
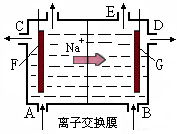
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.F电极材料为金属铁
参考答案:D
本题解析:根据装置图可知,在溶液中阳离子钠离子向右侧移动,所以G电极是阴极,F电极是阳极。所以氢离子在右侧生成,氯气在左侧生成。由于F是阳极,所以不能用活性电极铁作阳极。因此正确的答案是D。
本题难度:一般
3、简答题 工业上生产氯气,常用电解槽中电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.下图(左图)为电解槽的示意图.
(1)这种阳离子交换膜,只允许溶液中的______通过.(填下列微粒的编号)
①H2②Cl2③H+④Cl-⑤Na+⑥OH-
(2)写出在电解过程中阳极发生的电极方程式:______.
(3)已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通.则理论上计算,电解后流出的氢氧化钠溶液的质量分数为______.
(4)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇.回答下列问题:
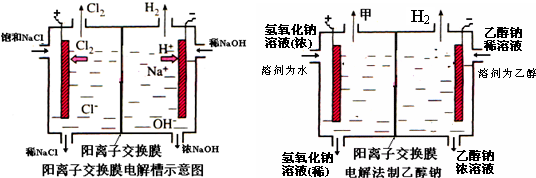
①写出在电解过程中阴极发生的电极方程式______.
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇钠固体的方法是:______.
参考答案:(1)阳离子交换膜只允许阳离子钠离子、氢离子通过,而阴离子和分子均不能通过,故答案为:③⑤;
(2)电解池中和电源的正极相连的是电解池的阳极,阳极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
(3)氢气的质量=VVmM=896L22.4L/mol×2g/mol=80g;电解水时,生成氢气与氢氧化钠的物质的量之比为1:2,所以生成氢氧化钠的质量=2896L22.4L/mol×40g/mol=3200g,溶液增加的质量为增加的钠元素的质量减去生成氢气的质量=2×896L22.4L/mol×23g/mol-80g=1760g;溶液中溶质氢氧化钠的质量为10000g×10%+3200g=4200g,溶液的质量为10000g+1760g=11760g,
电解后流出的氢氧化钠溶液的质量分数=4200g11760g×100%=35.7%,
故答案为:35.7%;
(4)①电解池中和电源的负极相连的是电解池的阴极,阴极上乙醇得电子发生还原反应,即2CH3CH2OH+2e-=2CH3CH2O-+H2↑.
故答案为:2CH3H2OH+2e-=2CH3CH2O-+H2↑;
?②从溶液中析出溶质的方法是蒸发结晶,故答案为:蒸发结晶.
本题解析:
本题难度:一般
4、选择题 如图为铁片上镀铜的实验装置,下列说法正确的是
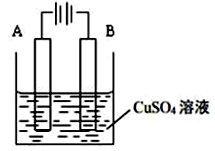
A.Cu2+在A极被还原
B.硫酸铜溶液浓度变小
C.铜片连接电源正极,铁片上发生还原反应
D.B极发生反应:Cu-2e-=Cu2+
参考答案:C
本题解析:A、A电极与电源的正极相连,作阳极,因此A电极应该是铜,铜失去电子。A不正确;B、电镀时溶液中的浓度是不变的,B不正确;C、电镀时待镀金属作阴极,镀层做阳极,所以铜片连接电源正极,铁片连接电源的负极,铁片上铜离子得到电子,发生还原反应,C正确;D、B电极是阴极,溶液中的铜离子得到电子,电极反应式为Cu2++2e-=Cu,D不正确,答案选C。
本题难度:一般
5、填空题 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" ―1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=" ―566" kJ/mol
则表示甲烷燃烧热的热化学方程式 。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是: 。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据: CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
| H2O
| CO
| CO2
| 1
| 650
| 2
| 4
| 1.6
| 5
| 2
| 900
| 1
| 2
| 0.4
| 3
| 3
| 900
| 1
| 2
| 0.4
| 1
|
①实验1中,以v (H2)表示的平均反应速率为 。
②实验3跟实验2相比,改变的条件可能是 (答一种情况即可)
参考答案:(1)CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1 CO2(g)+2H2O(l) △H1=―890KJ.mol-1
(2)CH4-8e-+ 10 OH- CO32-+ 7H2O; CO32-+ 7H2O;
(3) B、D ;
(4)① 0.16mol/(L・min) ②使用了催化剂;加大了压强(任答一种)
本题解析:(1)甲烷完全燃烧生成二氧化碳气体和液态水,所以甲烷燃烧热的热化学方程式中甲烷的物质的量是1mol,将①②相加除以2可得,答案是CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1 CO2(g)+2H2O(l) △H1=―890KJ.mol-1
(2)负极发生氧化反应,所以甲烷在负极发生氧化反应,结合电解质溶液,负极的电极反应式为CH4- 8e-+ 10 OH- CO32-+ 7H2O; CO32-+ 7H2O;
(3)A、电解过程中两极分别是H+和Fe放电生成氢气和亚铁离子,所以两极哪端都可以生成氢气,a不一定为正极,b不一定为负极,但a为正极,b为负极,效果较好,错误;B、在装置中铁一定作阳极,所以氯化钠溶液是电解质溶液,不影响阳极Fe放电生成亚铁离子,阴极H+放电生成氢气,正确;C、装置中铁一定作阳极,阴极可以是铁,也可以是其他惰性电极,错误;D、阴极H+放电生成氢气,正确,答案选BD。
(4)①实验1中,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= 0.8mol/L/5min=0.16mol/(L・min);
②实验3跟实验2相比,到达平衡时间缩短,说明反应速率加快,反应温度、各物质的物质的量均未变,所以可能是使用了催化剂或增大压强。
考点:考查盖斯定律得应用,电化学理论的应用,反应速率的计算及条件对反应速率的影响判断
本题难度:困难
|