1、填空题 (1)如图1表示某同学配制480mL?0.5mol/L?的NaOH溶液的部分操作示意图,其中有错误的是______,这样操作所配制的溶液比要求的浓度要______?(填“偏高”、“偏低”、“不影响”) www.91exAm.org.
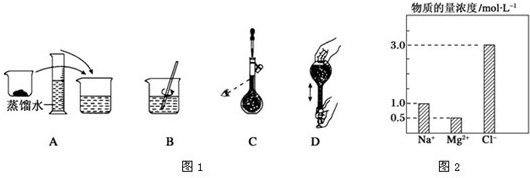
(2)在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图2所示,回答下列问题:
该混合液中,NaCl的物质的量浓度为______
含溶质MgCl2的物质的量为______
含溶质CaCl2的质量为______
将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为______.
参考答案:(1)定容时眼睛与刻度线相平,不能俯视或仰视;定容时,眼睛仰视刻度线,溶液的液面超过刻度线,溶液的体积偏大,浓度偏小,故答案为:C;?偏低;
(2)NaCl的物质的量浓度=钠离子浓度=1.0?mol?L-1;根据MgCl2的物质的量浓度=镁离子浓度=0.5?mol?L-1,MgCl2的物质的量=0.5?mol?L-1×0.2L=0.1mol,溶液中的电荷守恒:c(Na+)×1+c(Mg2+)×2+c(Ca2+)×2=c(Cl-)×1,
1.0?mol?L-1 +0.5?mol?L-1×2+c(Ca2+)×2=3?mol?L-1×1,c(Ca2+)=0.5?mol?L-1,c(CaCl2)=0.5?mol?L-1,溶质CaCl2的质量为0.5?mol?L-1×0.2L×110g/mol=11.1?g;稀释后溶液中Ca2+的物质的量浓度为0.5?mol?L?-1×0.2L1L=0.1?mol?L-1;故答案为:1.0?mol?L-1;0.1mol;11.1g;0.1?mol?L-1.
本题解析:
本题难度:一般
2、选择题 表示阿伏加德罗常数,下列判断正确的是
A.在18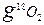 中含有
中含有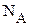 个氧原子
个氧原子
B.标准状况下,22.4L空气含有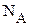 个单质分子
个单质分子
C.1 mol 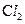 参加反应转移电子数一定为2
参加反应转移电子数一定为2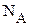
D.含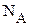 个
个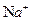 的
的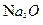 溶解于1L水中,
溶解于1L水中,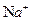 的物质的量浓度为1 mol・
的物质的量浓度为1 mol・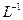
参考答案:A
本题解析:略
本题难度:一般
3、选择题 在科学实验和工农业生产中,所使用的一定量的溶液一般都是量取它的体积,而较少称量它的质量。在溶液中发生的化学反应,反应物和生成物的物质的量也存在一定的比例关系。因此我们引入一个新的物理量--物质的量浓度来建立物质的量和溶液体积的关系。认真分析物质的量浓度的概念及其定义式并思考,下列溶液中溶质的物质的量浓度为1mol/L的是
[? ]
A.将40gNaOH溶解于1L水中
B.将22. 4L氯化氢气体溶于水配成1L溶液
C.将1L 10mol/L的浓盐酸与9L水混合
D.将10gNaOH溶解于水中配成250mL溶液
参考答案:D
本题解析:
本题难度:简单
4、选择题 在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的体积和乙的体积相同
D.甲的相对分子质量比乙的相对分子质量小
参考答案:B
本题解析:在相同条件下,气体的密度之比是相应气体的摩尔质量之比,所以甲的摩尔质量大于乙的摩尔质量。则在质量相等的条件下,甲的物质的量小于乙的物质的量,所以选项B正确,其余都是不正确的,答案选B。
本题难度:一般
5、计算题 (4分)某化学研究性学习小组对含有杂质的铁粉样品进行分析(杂质不与酸反应)。
实验序号
| 加入盐酸体积/mL
| 剩余固体质量/g
|
1
| 10
| 1.8
|
2
| 20
| 1.1
|
3
| 30
| 0.5
|
4
| 50
| 0.5
|
取4份质量均为2.5g的样品,分别与同一浓度的盐酸反应,实验结果记录如右表。试计算:
(1)每份样品中所含杂质的质量为 g。
(2)所用盐酸溶液的物质的量浓度为 mol?L-1。
参考答案:0.5g 2.5mol/L
本题解析:略
本题难度:困难