1、选择题 下列说法正确的是
A.H2O和H2O2中的化学键类型完全相同
B.N2的结构式为N―N
C.一个D2O分子所含的中子数为10(质量数:D-2,O-16)
D.NaCl的电子式为
参考答案:C
本题解析:A中双氧水还含有非极性键,A不正确;氮气中含有三键,结构式为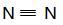 ,B不正确;氯化钠是含有离子键的离子化合物,电子式为
,B不正确;氯化钠是含有离子键的离子化合物,电子式为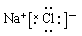 ,D不正确,所以正确的答案选C。
,D不正确,所以正确的答案选C。
本题难度:简单
2、选择题 下列各组为两种元素的原子序数,其中不能反应生成AB3型化合物的是:
A.13和17
B.16和8
C.9和3
D.15和17
参考答案:C
本题解析:A可以生成AlCl3,B可以生成SO2,C可以生成LiF,D可以生成PCl3,所以答案是C。
本题难度:简单
3、选择题 下列判断正确的是?(?)
A.元素周期表中查得的相对原子质量为同使素的相对原子质量
B.化学键的变化一定会引起化学反应的变化
C.酸性氧化物一定是非金属氧化物
D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
参考答案:B
本题解析:略
本题难度:一般
4、选择题 下列说法中错误的是
A.原子及其离子的核外电子层数等于该元素所在的周期数;
B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素;
C.除氦外的稀有气体原子的最外层电子数都是8;
D.同一元素的各种同位素的物理性质、化学性质均相同
参考答案:AD
本题解析:A不正确,例如钠离子的核外电子层数是2层,但钠是第三周期元素。质子数相同,中子数不同的同一种元素的不同核素互称为同位素,所以互为同位素的原子物理性质不同,化学性质相似,D不正确,答案选AD。
本题难度:一般
5、选择题 已知W、X、Y、Z是短周期元素,aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列说法正确的是
A.离子的还原性:Y2-> Z-
B.原子半径:r(W) > r(X)
C.质子数:c>a
D.W和X两者最高价氧化物对应的水化物能相互反应
参考答案:A
本题解析:依题意推断,四种离子具有28电子层结构,aW2+、bX+、cY2-、dZ-分别为12Mg2+、11Na+、8O2-、9F-,则W、X、Y、Z分别为Mg、Na、O、F;非金属性:O<F,则单质的氧化性:O2<F2,由氧化还原反应规律可知,还原性:8O2->9F-,故A正确;原子半径:Na>Mg,离子半径:Na+> Mg2+,故B错误;c=8,a=12,8<12,则c<a,故C错误;氢氧化镁是中强碱,不是两性氢氧化物,氢氧化钠是强碱,二者不能反应,故D错误。
本题难度:一般