1、填空题 氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.已知pH为5时,+2价铜已开始以碱式盐的形式沉淀.某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:
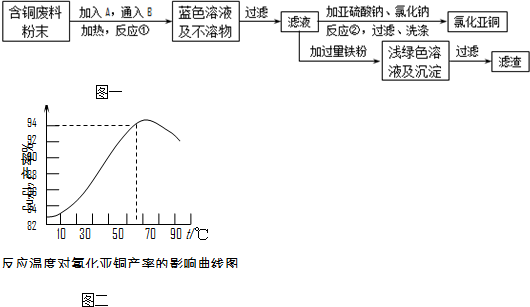
(1)加入的A是______,通入的B是______.
(2)反应②的离子方程式是______.为提高Cu2Cl2的产率,常在反应②的溶液中加适量稀碱溶液,控制pH为3.5.这样做的目的是______.
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在______时,Cu2Cl2的产率已达到94%,当温度高于65℃时,Cu2Cl2产率会下降,其原因可能是______.
参考答案:(1)金属铜和稀硫酸不反应,但是在鼓入空气的条件下会发生反应生成硫酸铜,所以A是稀硫酸,B是空气,
故答案为:稀硫酸;空气;
(2)由图示可知,反应物有:Cu2+、SO32-、Cl-,生成物有Cu2Cl2、SO42-,由于是氧化还原反应,化合价发生了变化,根据电子得失和质量守恒进行配平:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+,在反应②的溶液中加适量稀碱溶液,OH-中和了反应中的H+,有利于平衡向右进行,提高Cu2Cl2的产率,但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了Cu2Cl2的产率,,故答案为:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+;OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率,但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯;
(3)因在60℃时CuCl产率最大,根据信息可知,随温度升高,促进了Cu2Cl2的水解,Cu2Cl2被氧化的速度加快.
故答案为:温度过高,促进了CuCl2的水解.
本题解析:
本题难度:简单
2、实验题 盐酸、硝酸都是用途相当广泛的两种酸。
(1)瑞典科学家舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种黄绿色气体。写出该反应的化学方程式,并用双线桥方法表示电子转移关系和数目: ? ? 。
(2)某校合作学习探究小组学习科学家探究精神对氯气性质进行了探究,设计了以下一些实验。

①能说明氯气与水发生化学反应的实验是? (填实验序号)
②写出实验D中所发生反应的离子方程式? 。
(3)该校另一合作学习探究小组用下左图所示装置对铜与硝酸反应进行探究。
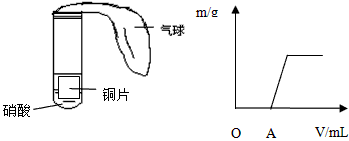
①甲同学观察到试管中的气体由无色变成了红棕色,由此认为试管里的硝酸是浓硝酸,你认为他的看法正确吗?? 。为什么?? ? 。甲同学还能观察到的现象有?? 。
②乙同学向反应完成后的溶液里滴加氢氧化钠溶液,产生的沉淀(m/g)和加入溶液的体积(V/mL)的关系如上右图所示。请写出O-A段反应的离子方程式? 。
参考答案:(1)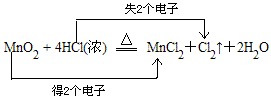
(2)①BC;②Cl2+2OH-==Cl-+ClO-+H2O
(3)①不正确;因为一氧化氮与试管内空气中的氧气反应,也会产生红棕色气体;气球鼓起胀大,铜片上放出气泡,溶液由无色变成蓝色,铜片变小甚至消失(至少答出两种现象)
? ?②H++OH-==H2O
本题解析:
本题难度:困难
3、选择题 下列叙述正确的是
[? ]
A.Na2O2、Cl2、NO2均能与水发生氧化还原反应
B.在加热的条件下稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
C.Cu、Fe、C分别在氧气中燃烧都只能生成一种氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
参考答案:A
本题解析:
本题难度:简单
4、选择题 将W1g光亮的铜丝在空气中加热一段时间后,迅速插入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥、称得其质量为W2g。实验时由于所插入的物质不同,钢丝的前后质量变化可能不同,下列所插物质与铜丝的质量变化关系不正确的是
[? ]
A.石灰水:W1<W2
B.CO:W1=W2
C.NaHSO4:W1 >W2
D.乙醇溶液:W1<W2
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是
[? ]
①C与O2②Na与O2③Fe与Cl2④AlCl2溶液与氨水⑤CO2与NaOH溶液⑥Cu与硝酸⑦AgNO3溶液与氨水
A.除③外
B.除③⑦外
C.除③④外
D.除⑥⑦外
参考答案:C
本题解析:
本题难度:简单