1、选择题 科学的假设与猜想是科学探究的先导和价值所在,下列假设或猜想引导下的探究肯定没有意义的是( )
A.探究SO2和Na2O2反应可能有Na2SO4生成
B.探究Na与水的反应可能有O2生成
C.探究浓硫酸与铜在一定条件下反应生成的黑色物质可能是CuO
D.探究向滴有酚酞试液的NaOH溶液中通入Cl2,溶液红色褪去的现象是溶液的酸碱性改变,还是HClO的漂白性所致
参考答案:A、二氧化硫具有还原性,过氧化钠具有氧化性,所以可以探究SO2和Na2O2反应可能有Na2SO4生成,故A不选;
B、根据质量守恒定律,化学反应前后元素的种类不变,钠和水中含有钠元素、氢元素和氧元素,猜测产生的气体可能为氧气,不符合氧化还原反应的基本规律,钠是还原剂,水只能做氧化剂,元素化合价需要降低,氧元素已是最低价-2价,不可能再降低,故B选;
C、浓硫酸与铜发生氧化还原反应,铜有可能被氧化为黑色的氧化铜,有探究意义,故C不选;
D、氯气和氢氧化钠反应生成氯化钠次氯酸钠和水,消耗氢氧化钠溶液红色褪去,氯气可以与水反应生成的次氯酸或生成的次氯酸钠水解生成次氯酸具有漂白性,有探究意义,故D不选;
故选B.
本题解析:
本题难度:一般
2、填空题 (6分)现有12. 4 g 金属钠与过氧化钠的固体混合物,把该混合物分多次投入水中,充分反应后产生的两种气体可恰好完全反应。
(1)两种气体的质量比为_____________________
(2)求原固体混合物中过氧化钠的质量____________________(结果保留两位小数)
参考答案:(1)m(H2):m(O2)==1:8? (2分)?(2)7.80 (4分)
本题解析:略
本题难度:一般
3、选择题 将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,得到溶质质量分数分别为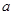 %和
%和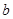 %的两种溶液,则
%的两种溶液,则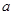 和
和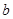 的关系是
的关系是
A.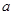 =
=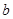
B.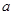 >
>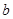
C.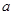 <
<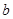
D.无法确定
参考答案:A
本题解析:等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,生成的氢氧化钠的物质的量相同,即溶液中溶质的质量相同,对于反应 ;1mol氧化钠与足量的水反应,溶液质量增加62g,对于反应
;1mol氧化钠与足量的水反应,溶液质量增加62g,对于反应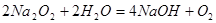 ,1mol过氧化钠与足量的水反应,溶液的质量增加62g,所以反应物两溶液的质量相同,即,则
,1mol过氧化钠与足量的水反应,溶液的质量增加62g,所以反应物两溶液的质量相同,即,则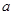 和
和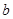 的关系是
的关系是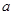 =
=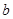
本题难度:一般
4、实验题 (15分)为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案:
(1)方案一:称取一定质量的样品(10g),置于坩埚中加热至恒重,冷却,称取剩余固体质量为10.8g,计算。①实验中加热至恒重的目的是?。(2分)②样品中Na2CO3的质量分数为?(2分)
(2)方案二:以下图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)

①已知仪器C中装有品红溶液,其作用是______________(2分),有人提出该溶液可能引起Na2CO3含量的测量结果比实际值偏低,理由是____________________。(2分)
②实验室中备有以下常用试剂:a.浓硫酸? b.品红溶液? c.酸性高锰酸钾溶液d.氢氧化钠溶液? e.无水硫酸铜? f.碱石灰? g.五氧化二磷? h.无水氯化钙?请将下列容器中应盛放的试剂序号填入相应空格:B中______,D中________,E中________。(各1分)
③实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的氮气。这样做的目的是______________。(2分)
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量BaCl2溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗干净的方法是_________。 (2分)
参考答案:
本题解析:略
本题难度:一般
5、选择题 下列说法不正确的是(?)
A.干燥的氯气可以用钢瓶运输
B.钠可以保存在CCl4液体中
C.Na2O2可作为潜水艇的供氧剂
D.实验后剩余的钠粒可放回原试剂瓶中
参考答案:B
本题解析:A、常温下,干燥的氯气与铁不反应,可以用钢瓶运输,正确;B、钠的密度比CCl4的密度小,浮在CCl4液体的表面上,起不到隔绝空气的作用,错误;C、Na2O2可与二氧化碳、水蒸气反应产生氧气,可作为潜水艇的供氧剂,正确;D、实验后剩余的钠粒可放回原试剂瓶中,正确。
本题难度:简单