1、填空题 下表列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
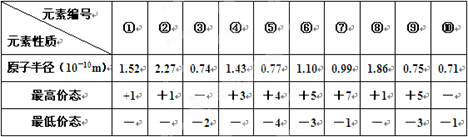
根据元素的主要化合价和原子半径可知,①~⑩分别是Cl、K、O、Al、C、P、Na、N、F。
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是?(填写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)?。某元素R的原子半径为1.02×10-10m,该元素在周期表中位于?;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式?。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为?。
2、填空题 晶体是质点(分子、离子或原子等)在空间有规则地排列、具有整齐外形、以多面体出现的固体物质。在空间里无限地周期性的重复能形成晶体的、具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如下图所示。
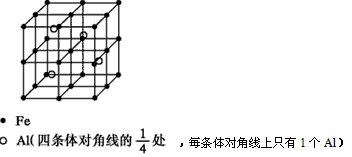
请据此回答下列问题:
(1)确定该合金的化学式____________。
(2) 若晶体的密度为ρ g/cm3,NA为阿伏加德罗常数,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为____________cm。
3、选择题 下列说法正确的是?
A.制普通玻璃的主要原料是烧碱、石灰石、石英
B.常用氢氟酸(HF)来刻蚀玻璃
C.用带玻璃塞的试剂瓶保存NaOH溶液
D.光导纤维的主要成分是硅
4、填空题 离子键的强弱主要决定于离子半径和离子的电荷值。一般规律是:离子半径越小,电荷值越大,则离子键越强。试分析:①K2O?②CaO?③MgO 的离子键由强到弱的顺序是?(4分)
5、选择题 某下列叙述错误的是(?)
A.金属单质或合金在固态或液态时都能导电
B.金属晶体中的自由电子属整个晶体共有
C.晶体中只要存在离子,则一定是离子晶体
D.金属镁比金属钠的熔点高,因为镁中阳离子与自由电子之间的作用力强