1、选择题 化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.二氧化硅是光纤制品的基本原料
B.水玻璃可用作黏合剂和防火剂
C.电解NaCl饱和溶液,可制得金属钠
D.Al2O3的熔点很高,是一种耐火材料
参考答案:C
本题解析:电解饱和的氯化钠溶液,生成物是氢氧化钠、氢气和氯气,电解熔融的氯化钠才能得到金属钠,选项C不正确,其余选项都是正确的,答案选C。
点评:该题常识性知识的考查,难度不大,学生只要熟练记住即可。本题有利于培养学生的学习兴趣,调动学生的学习积极性。
本题难度:简单
2、选择题
方案1 :向废液中加入过量的铁粉,充分反应后,过滤。?在所得滤渣中加入足量的盐酸,充分反后,再过滤即得到铜。
方案1中涉及的四种阳离子的氧化牲由强到弱的顺序为:_____________________过滤操作时,需要用到的玻璃仪器是:______________________
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的Cu已全部析出。
方案2中铜作______极,所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)_______________________________________________________?另一电极所发生的电极反应为_____________________________?方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为: ______________________
参考答案:①方案1:Fe3+>Cu2+>H+>Fe2+?漏斗、烧杯、玻璃棒方案2:阴? 2Fe3++2e-=2Fe2+;? Cu2++2e-="Cu" ;2H++2e-=H2↑;? 2Cl--2e-=Cl2↑有污染性气体Cl2产生?②使用了电解装置,成本较高等。
本题解析:本题以废液中回收Cu为素材,将氧化还原反应知识和电化学知识紧密的结合起来,方案1中同时考查了过滤操作。方案2是用电解的方法回收Cu,用铜和石墨作电极,铜要做阴极,阳离子在阴极得电子,因溶液中含有Fe3+、Cu2+、H+、Fe2+,所以存在得电子顺序问题,由方案1中知氧化性由强到弱的顺序为Fe3+>Cu2+>H+>Fe2+,故得电子顺序为Fe3+>Cu2+>H+>Fe2+,由题意知Fe3+、Cu2+、H+分别先后在阴极得电子。最后一问还从环保和经济方面考查了方案的不足。
本题难度:一般
3、计算题 (4分)常温下,要将质量分数为10%的氯化钠溶液100g变为质量分数为20%的氯化钠,常用的方法有加入溶质和蒸发溶剂。请通过计算回答:
⑴需要加入氯化钠晶体?g。?
⑵需要蒸发掉?g水。
参考答案:⑴12.5g。?⑵50g
本题解析:(1)设需要加入氯化钠的质量是m,则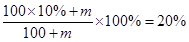 ,解得m=12.5g。
,解得m=12.5g。
(2)设需要蒸发的溶剂质量是n,则根据蒸发过程中溶质不变可知,100×10%=(100-n)×20%,解得n=50g。
本题难度:简单
4、选择题 常温常压下,将一定质量的Fe、Fe2O3、Fe3O4的混合物平均分成两份,一份溶于足量稀硝酸中恰好完全反应,生成0.1 mol NO气体, 将另一份溶于足量稀盐酸中生成一定量气体,向两次反应后溶液中加入硫氰化钾溶液,溶液颜色均无明显变化,则固体溶于盐酸后生成气体的体积为(?)
A.2240mL
B.3360mL
C.3675mL
D.4480mL
参考答案:C
本题解析:根据题意可知,反应后的溶液是含有Fe2+的溶液。硝酸与Fe、Fe2O3、Fe3O4的混合物反应产生Fe(NO3)2、NO、H2O。Fe、Fe2O3、Fe3O4的混合物与元素反应产生FeCl2、H2、H2O。假设每一等分含有Fe、Fe2O3、Fe3O4的物质的量分别是a、b、c,则根据电子守恒可得2a=2b+2c+0.1×3;假设产生的氢气的物质的量为x,在另一份中的电子守恒是:2a=2b+2c+2x。2x=0.3.所以x=0.15mol。该气体在标准状况下体积是V=n・Vm=0.15mol×22.4L/mol=3.36L=3360ml,若在常温下,因为温度高于标准状况,所以气体摩尔体积比22.4L/mol略大,所以放出的气体的体积就比3360ml稍微大些,只有C符合题意。故选项是C。
本题难度:一般
5、选择题 在某种不纯的铁片中,可能含有Mg、Al、Cu等金属杂质。取这种铁片5.6 g,跟足量稀盐酸反应,得到2.24 L(标准状况)H2,则该铁片中(?)
A.一定不含镁
B.一定不含铝
C.一定含有铜
D.一定含有镁、铝、铜
参考答案:C
本题解析:R+2H+====R2++H2↑
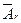 ?1
?1
5.6 g? 0.1 mol
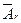 =56
=56
Al若转换成+2价,相对原子质量为18,Cu不反应,相对原子质量为64。
因Mg的相对原子质量Ar(Mg)<56,故一定不含Al,一定含有Cu。
本题难度:简单