1、选择题 加热NH4HCO3固体,使产生的气体依次通过盛有过量Na2O2的干燥管、浓H2SO4的洗气瓶,最后得到的气体是(?)
A.NH3
B.CO2
C.O2
D.CO2与O2
参考答案:C
本题解析:NH4HCO3分解反应的方程式为:NH4HCO3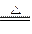 NH3↑+H2O↑+CO2↑。H2O与CO2通过过量Na2O2发生反应生成O2,NH3和O2的混合气体通过浓H2SO4,NH3被吸收,最后得到的气体是O2。
NH3↑+H2O↑+CO2↑。H2O与CO2通过过量Na2O2发生反应生成O2,NH3和O2的混合气体通过浓H2SO4,NH3被吸收,最后得到的气体是O2。
本题难度:简单
2、选择题 某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或二种。现将13.8 g样品加入足量水,样品全部溶解。再加入过量的CaCl2溶液,得到9 g沉淀。对样品所含杂质的正确判断是
A.肯定有KNO3
B.肯定有KNO3,可能还含有Na2CO3
C.肯定没有Ba(NO3)2,可能有KNO3
D.肯定没有Na2CO3和Ba(NO3)2
参考答案:AB
本题解析:将13.8 g样品加入足量的水,样品全溶解则样品中一定无Ba(NO3)2(因能与K2CO3生成沉淀)。下面用中值法分析:如13.8 g是纯的K2CO3,则生成CaCO3沉淀应为10 g,而现在得沉淀9 g,则混进的杂质或不与CaCl2生成沉淀,或13.8 g杂质与CaCl2作用生成的沉淀小于9 g。杂质中KNO3不与CaCl2生成沉淀,符合题意。而13.8 g Na2CO3与CaCl2混合生成沉淀为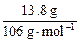 ×100 g・mol-1>9 g不合理。所以选项A正确。但分析选项B,可能存在这样的情况,即混进很多的KNO3,而只混进少量的Na2CO3,这时也可以保证13.8 g样品与CaCl2反应后只生成9 g沉淀,故B也正确。此题考查学生思维的严密性。选项B很容易漏掉。
×100 g・mol-1>9 g不合理。所以选项A正确。但分析选项B,可能存在这样的情况,即混进很多的KNO3,而只混进少量的Na2CO3,这时也可以保证13.8 g样品与CaCl2反应后只生成9 g沉淀,故B也正确。此题考查学生思维的严密性。选项B很容易漏掉。
本题难度:简单
3、选择题 下列关于氧化钠和过氧化钠的说法不正确的是
A.过氧化钠比氧化钠稳定
B.氧化钠是白色固体,过氧化钠是淡黄色固体
C.均属于碱性氧化物
D.均与CO2反应
参考答案:C
本题解析:能跟酸反应只生成盐和水的氧化物叫碱性氧化物,氧化钠跟属于碱性氧化物,过氧化钠跟酸反应除生成盐和水外,还有氧气,不属于碱性氧化物。
本题难度:一般
4、选择题 有甲、乙、丙、丁四个烧杯均盛100 mL水,现向四个烧杯中分别放入等质量的Na、Na2O、Na2O2、NaOH(水均足量),所得溶液的质量分数由大到小的顺序为(?)
A.甲>乙>丙>丁
B.乙>丙>甲>丁
C.乙=丙>甲>丁
D.丁>甲>乙>丙
参考答案:A
本题解析:因为四种物质中,Na中,Na元素质量分数最大(100%),NaOH中Na元素质量分数最小(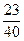 ),故所得溶液中溶质含量甲中最多,丁中最少,只有A选项符合。
),故所得溶液中溶质含量甲中最多,丁中最少,只有A选项符合。
本题难度:简单
5、选择题 下列各组物质混合后,不能生成NaOH的是
A.Na和H2O
B.Na2O2和H2O
C.Ca(OH)2溶液和Na2CO3溶液
D.Ca(OH)2溶液和NaCl溶液
参考答案:D
本题解析:钠和水反应生成氢氧化钠和氢气,过氧化钠和水反应生成氢氧化钠和氧气,Ca(OH)2溶液和Na2CO3溶液反应生成碳酸钙和氢氧化钠,D中物质不反应,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,同时兼顾学生能力的培养,难度不大,记住常见的化学反应即可。
本题难度:简单