1、选择题 用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是(? )

A.电子通过盐桥从乙池流向甲池
B.铜导线替换盐桥,原电池仍继续工作
C.开始时,银片上发生的反应是:Ag-e-=Ag+
D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
参考答案:D
本题解析:根据原电池工作原理,电子由负极(Cu)沿导线传递给正极(Ag),电解质溶液中阴离子沿盐桥从乙流向甲;正极(Ag):2Ag++2e-=2Ag,负极(Cu):Cu-2e-=Cu2+,总反应:Cu+2Ag+=Cu2++2Ag,与将Cu片浸入AgNO3溶液中发生的化学反应相同。故选D。
本题难度:一般
2、计算题 按下图装置进行实验,并回答下列问题
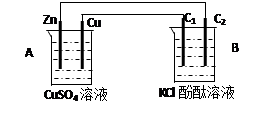
(1)判断装置的名称:B池为
(2)铜极为______极,电极反应式为
石墨棒C2附近发生的实验现象为
(3)当C2极析出224mL气体(标准状态时,锌的质量变化(增加或减少) g.
CuSO4溶液的质量变化了(增加或减少了) g .
参考答案:(共9分,前3空每空1分,其余各2分)
(1) 电解池 (2)正 Cu2+ + 2e- = Cu 有气泡冒出,溶液变红
(3)减少 0.65 增加 0.01
本题解析:(1)锌能和硫酸铜发生置换反应,所以根据装置结构特点可知,A是原电池,则B就是电解池。
(2)铜是正极,溶液中的铜离子得到电子,电极反应式是Cu2+ + 2e- = Cu。石墨棒C2和电源的负极相连,做阴极,溶液中的氢离子放电,同时破坏溶液中水的电离平衡,使阴极周围溶液显碱性,所以附近发生的实验现象为有气泡冒出,溶液变红。
(3)224ml气体是氢气,物质的量是0.01mol,则转移0.02mol电子,所以根据电子的得失守恒可知,消耗锌的物质的量是0.02mol÷2=0.01mol,质量是0.65g,即锌的质量减少0.65g。由于正极析出铜的质量是0.64g,所以溶液质量增加0.65g-0.64g=0.01g。
考点:考查原电池和电解池的有关判断和计算
点评:该题是中等难度的试题,也是高考中的常见考点,试题基础性强,难易适中。主要是考查学生对电化学原理的了解掌握程度,有助于培养学生的逻辑思维能力,提高学生分析问题、特别是灵活运用基础知识解决实际问题的能力。
本题难度:一般
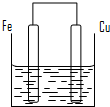
3、简答题 将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置.
(1)铁片上的电极反应式为______,铜片周围溶液会出现______的现象.
(2)若2min后测得铁片和铜片之间的质量差为1.2g,则导线中流过的电子为______mo1,该段时间内用硫酸铜表示的平均反应速率为______
(3)若一段时间后测得铁片减少了2.4g,同时铜片增加了3.2g,则这段时间内该装置消耗的化学能有______%转化为电能.
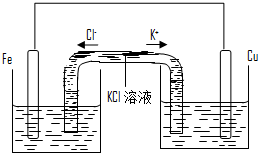
(4)若将该装置改为如下图所示的装置也能达到和原装置相同的作用,同时能保证停止使用该装置时反应物不损耗,KCl溶液起沟通两边溶液形成闭合回路的作用,则硫酸铜溶液应该注入______(填“左侧”、“右侧”或“两侧”)烧杯中,若2min内铁片减少了2.8g,则中间U形管中K+的流速是______mo1/min.(以上均假设反应过程中溶液体积不变).
参考答案:(1)装置没有外加电源,属于原电池,活泼金属锌做负极,本身失电子,Fe-2e-=Fe2+,正极上是铜离子得电子,所以铜离子在该极附近溶度减小,溶液颜色变浅,故答案为:Fe-2e-=Fe2+;颜色变浅;
(2)铁电极发生的反应为:Fe-2e-→Fe2+,正极上是铜离子得电子,电极反应为:Cu2++2e-=Cu,设转移电子为n,则铁质量减少28n,Cu电极质量增加32n,铁片和铜片之间的质量差为28n+32n=60n=1.2g,所以n=0.02mol,所以铜离子浓度减少量为0.01mol,所以该段时间内用硫酸铜表示的平均反应速率v=0.01mol0.5L2min=0.01mol?L-1?min-1,故答案为:0.02;0.01mol?L-1?min-1;
(3)铁电极的电子一部分传给铜电极,发生原电池反应.同时铁电极上也发生置换反应.电极反应:Fe-2e-→Fe2+,Cu2++2e-=Cu,铜电极增加3.2g,即0.05mol,同时铁电极原电池反应产生0.05molFe2+,即铁电极减少56g/mol×0.05
mol=2.8g,但是铁片只减少了2.4g,因为铁片有一部分直接发生置换反应,有铜生成,所以质量增加了,这部分铁的化学能没有转化为电能,所以有2.8g-2.4g=0.4g的质量差,设有xmol铁直接参与置换反应,
Cu2++Fe=Cu+Fe2+△m
? 1mol 64?8
? ?x?0.4
计算得x=0.05mol,即直接发生置换反应的铁为0.05mol,参与原电池反应的铁也是0.05mol,所以该装置消耗化学能有50%转化为电能,故答案为:50;
(4)盐桥原电池中,金属电极插入含有该电极金属阳离子的盐溶液中,所以硫酸铜溶液应该注入右侧烧杯中,若2min内铁片减少了2.8g,该段时间内用亚铁离子表示的平均反应速率v=2.8g56g/mol0.5L2min=0.05mol?L-1?min-1,则中间U形管中K+的流速是0.05mo1/min,故答案为:右;0.05.
本题解析:
本题难度:一般
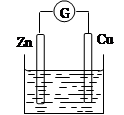
4、选择题 如右图所示装置,若要使装置中电流计的指针发生偏转,则向容器中加入的物质是
A.植物油
B.酒精
C.蔗糖溶液
D.稀硫酸
参考答案:D
本题解析:构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入电解质溶液中,ABC都是都不是电解质,硫酸是电解质,所以正确的答案选D。
本题难度:简单
5、选择题 铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=?Fe(OH)2+2Ni(OH)2下列有关该电池的说法正确的是?
[? ]
A.?电池的电解液为碱性溶液,阴极为Ni2O3、阳极为Fe ?
B.?电池放电时,负极反应为Fe+2OH-?+2e-=Fe(OH)2 ?
C.?电池充电过程中,阴极附近溶液的pH升高
D.?电池充电时,阴极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
参考答案:C
本题解析:
本题难度:一般