1、选择题 NA代表阿伏加德罗常数值,下列说法正确的是
A.78gNa2O2所含有的离子数为3NA
B.1mol甲基中含有电子数为10NA
C.7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
D.1molC10H22分子中共价键总数为22NA
参考答案:A
本题解析:A:Na2O2所含有的离子为Na+及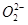 ,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
B:甲基为中性原子团,含有9个电子,故1mol甲基中含有电子数为9NA
C:氯气与碱液发生的是自身氧化还原反应:Cl2+2NaOH=NaCl+NaClO+H2O,只有一个电子转移,故7.1g氯气(0.1mol)与足量NaOH溶液反应转移的电子数为0.1NA
D:1molC10H22分子中共价键总数为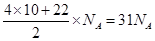
答案为A
本题难度:简单
2、选择题 设NA为阿佛加德罗常数,下列叙述中正确的是
A.标准状况下,22.4LSO2和O2混合气体中含有的氧原子数为2NA
B.0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA
C.2mol SO2和1mol O2在密闭容器中加热(V2O5催化)充分反应后,容器内气体分子总数为2NA
D.将0.1mol Cl2与足量NaOH溶液在常温下充分反应,转移的电子数为0.1NA
参考答案:AD
本题解析:本题考查阿伏加德罗常数与微粒间的关系,难度中等;标准状况下,22.4L混合气为1mol,其中含有氧原子为2mol,A项正确;0.1mol Fe在0.1mol C12中充分燃烧时,铁过量,氯气完全反应,故转移电子0.2mol,B项错误;SO2与 O2的反应为可逆反应,反应不能进行彻底,容器内分子数大于2NA,C项错误;0.1mol Cl2与足量NaOH溶液常温下反应,转移电子0.1mol,D项正确。
本题难度:一般
3、选择题 在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温、同压下,两容器内的气体一定具有相同的
[? ]
A.原子数?
B.密度
C.质量?
D.质?子数
参考答案:A
本题解析:
本题难度:简单
4、选择题 设以代表阿伏加德罗常数,下列说法正确的是?(?)
A.31 g白磷所含共价键数目为4NA
B.2 L pH=1的盐酸与醋酸溶液中氢离子数均为0.2 NA
C.标准状况下,2.24L C4H6所含碳原子数为0.6 NA
D.标准状况下,22g CO2含有的电子数为0.5 NA
参考答案:B
本题解析:略
本题难度:简单
5、选择题 若NA表示阿伏伽德罗常数,下列叙述中正确的是?
A.1mol含8个碳原子的某烃分子,最多形成8mol碳碳单键
B.标况下,100g含氢质量分数为12%的C2H4和甲醛的混合气体中氧原子数为NA
C.1 mol Cl2发生反应时,转移的电子数一定是2NA
D.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA
参考答案:B
本题解析:A 错误,最多形成7mol碳碳单键
B 正确。
C 错误,1 mol Cl2发生反应时,转移的电子数也可能是NA
D 错误,阴、阳离子总数为0.2NA
本题难度:一般