1、选择题 下列叙述正确确的是(? )
A.48gO3和O2的混合气体中含有6.02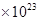 个分子
个分子
B.常温常压下,4.6gNO2气体含有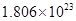 个原子
个原子
C.0.5mol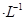 1LCuCl2溶液中含有
1LCuCl2溶液中含有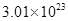 个Cu2+
个Cu2+
D.标准状况下,3.36LH2O含有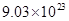 个分子H2O
个分子H2O
参考答案:B
本题解析:A、48gO3和O2的混合气体中含有3×6.02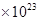 个氧原子,但是氧气分子与臭氧分子为多少并求不出,错误;B、常温常压下,4.6gNO2气体为0.1mol,含有的原子数为
个氧原子,但是氧气分子与臭氧分子为多少并求不出,错误;B、常温常压下,4.6gNO2气体为0.1mol,含有的原子数为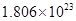 个,正确;C、铜离子会发生水解,因此溶液中的铜离子的物质的量小于
个,正确;C、铜离子会发生水解,因此溶液中的铜离子的物质的量小于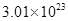 个,错误;D、水的质量不知道,无法确定,错误。
个,错误;D、水的质量不知道,无法确定,错误。
本题难度:简单
2、计算题 (8分)在100mL稀硫酸和稀盐酸的混合溶液中加入3.42g氢氧化钡固体,充分反应后(若溶液体积不变),过滤、干燥得沉淀2.33g,经测定滤液pH=13。试求原混合溶液中硫酸和盐酸的物质的量浓度分别是多少?
参考答案:c(H2SO4)= 0.1mol・L-1? c(HCl)= 0.1mol・L-1?(每空4分)
本题解析:略
本题难度:简单
3、选择题 下列叙述中正确的是
A.标准状况下,22.4LCO2和O2混合气体中含有6.02×1023个氧原子
B.常温常压下,0.1mol铁在0.1molCl2中充分燃烧,有1.806×1023个电子转移
C.一定条件下,2molSO2和1molO2反应达到平衡后,密闭容器内分子总数大于1.204×1024
D.1L1mol・L-1的K2CO3溶液中含有1.806×1024个离子
参考答案:C
本题解析:A项,混合气体含氧原子为2mol,A错;B项,氯气完全反应,而铁没有完全反应,转移电子数为0.2mol,B错;假设完全反应生成2molSO2,可逆反应不可能完全反应,平衡体系中,气体物质的量在2mol~3mol之间,C正确;D项,CO32-+H2O HCO3-+OH-,离子数增多,所以,1molK2CO3所含离子大于3mol,D错。故本题选C。
HCO3-+OH-,离子数增多,所以,1molK2CO3所含离子大于3mol,D错。故本题选C。
本题难度:一般
4、选择题 在Al2(SO4)3、MgSO4、K2SO4的混合溶液中,含有的Al3+、Mg2+、SO42-的个数比是2:3:8,则溶液中Al2(SO4)3、MgSO4、K2SO4的物质的量之比是( )
A.1:2:4
B.2:3:2
C.1:2:3
D.1:3:2
参考答案:溶液呈电中性,则阴阳离子所带电荷相等,设K+的个数与Al3+、Mg2+、SO42-的个数比是x:2:3:8,则x+2×3+3×2=2×8,所以x=4,同一溶液中离子的个数之比等于其浓度之比,再根据其化学式知Al2(SO4)3、MgSO4、K2SO4的物质的量浓度之比为22:3:42=1:3:2,同一溶液中各物质的物质的量之比等于其物质的量浓度之比,
故选D.
本题解析:
本题难度:简单
5、选择题 下列有关叙述正确的是( ? )
A.摩尔是国际科学界建议采用的一种物理量
B.物质的量是衡量物质所含原子数多少的物理量
C.H2的摩尔质量是2g
D.1molH2O含有2molH和1molO
参考答案:D
本题解析:
本题难度:一般