1��ѡ���� ����ԭ����������±��Ԫ�أ�����±�����ʵĵݱ���ɣ��������仯�������������ȷ���ǣ�������
A��KAt�˼�����KBr
B�����ڳ�����Ϊ��ɫ����
C��NaAt�۵�ϸ�
D����������ˮ���������Ȼ�̼
�ο��𰸣�A��±��Ԫ�ش��ϵ��£����Ӳ������࣬�뾶������KAt�˼�����KBr����A��ȷ��
B��±��Ԫ�ش��ϵ��£����ʵ���ɫ����۷е���������������ɫ���壬��B��ȷ��
C��±��Ԫ�������γɵĻ�����Ϊ���ӻ�����۵�ߣ���C��ȷ��
D�����������ڷǼ��Է��ӣ���������ˮ�������ڷǼ��Ե��л��ܼ�����D����
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� �����й�ԭ�ӽṹ��Ԫ�������ɵı�����ȷ����
��ԭ������Ϊ15��Ԫ�ص�ԭ�Ӱ뾶С��Nԭ�Ӱ뾶
�ڵڢ�A��Ԫ����ͬ�����зǽ�������ǿ��Ԫ��
�۵ڶ����ڵڢ�A��Ԫ�ص��⻯����ȶ��Դ���NH3
��ԭ������Ϊ12��Ԫ�ص�����������Ӧˮ����ļ��Դ���Al(OH)3
A.�٢�
B.�٢�
C.�ڢ�
D.�ۢ�
�ο��𰸣�C
���������ѡC�����⿼��ԭ�ӽṹ��Ԫ�������ɡ���ԭ������Ϊ15��Ԫ��Ϊ�ף���ԭ�Ӱ뾶����Nԭ�Ӱ뾶�����������ڱ��У�ͬһ���ڣ���������Ԫ�طǽ���������ǿ��±����ͬ�����зǽ�������ǿ��Ԫ�أ���ȷ���۵ڶ����ڵڢ�A��Ԫ����̼�������⻯��ΪCH4���ȶ���С��NH3������ԭ������Ϊ12��Ԫ����þ��Mg(OH)2�ļ��Դ���Al��OH��3����ȷ��
�����Ѷȣ�����
3������� �±��а��������֣�1��2������Ԫ�����ڱ����л��е���ţ������Ԫ��A��I�����ڱ��е�λ�ã��ش��������⣮
����
���� | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18
1
A
2
B
C
D
E
3
F
G
H
I
|
��1��B��C��Ԫ���зǽ����Խ�ǿ����______��д��Ԫ�����ƣ��������һ����ʵ��֤����һ����______��
��2������ijԪ�����γ����������д������������������������Һ�����ӷ�Ӧ����ʽ______��
��3��IԪ�������ڱ��е�λ���ǵ�______���ڡ���______�壮
��4������ijԪ�صĵ����ڳ�����Ϊ��̬����Ԫ������A��I�е�һ��Ԫ�ع���ԭ�Ӹ�����Ϊ1��1��2��1�����ֹ��ۻ�����X��Y����Ԫ�ػ�����A��I�е���һ��Ԫ�ع���ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ�����Z��M��д��Z��Y��Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣���Ԫ�������ڱ��е�λ�ÿ�֪��AΪ��Ԫ�أ�BΪ̼Ԫ�أ�CΪ��Ԫ�أ�DΪԪ�أ�EΪ��Ԫ�أ�FΪ��Ԫ�أ�GΪ��Ԫ�أ�HΪ��Ԫ�أ�IΪ��Ԫ�أ�
��1��ͬ����������ң��ǽ�������ǿ�����Էǽ���N��C��
ȡ̼���ƻ�̼��������Һ�����Թ��У������еμ�ϡ���ᣬ����ɫ��ζ�����������˵����������ǿ��N�ķǽ�����ǿ��
�ʴ�Ϊ������ȡ̼���ƻ�̼��������Һ�����Թ��У������еμ�ϡ���ᣬ����ɫ��ζ�����������˵����������ǿ��N�ķǽ�����ǿ��
��2������������ΪAl2O3����ǿ�Ӧ����ƫ�����κ�ˮ����Ӧ�����ӷ���ʽΪAl2O3+2OH-�T2AlO2-+H2O��
�ʴ�Ϊ��Al2O3+2OH-�T2AlO2-+H2O��
��3��I���ڵ����У���17�У�����I�������ڱ��е������ڣ���VIIA�壮
�ʴ�Ϊ������VIIA��
��4��XΪH2O2��YΪH2O����XΪCO��YΪCO2����ZΪNa2O2��MΪNa2O��
Na2O2��ˮ��Ӧ����NaOH����������Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O�T4NaOH+O2����
Na2O2��CO2��Ӧ����Na2CO3����������Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2CO2=2Na2CO3+O2��
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����2Na2O2+2CO2=2Na2CO3+O2��
���������
�����Ѷȣ�һ��
4���ƶ��� �����ֶ�����Ԫ��xA��yB��zC��mD��nE������x+y+z+m+n=57����֪AԪ�ص���̬�⻯����������������Ӧ��ˮ�����ڳ������ܻ��ϳ�һ�ֻ����CԪ�ص�ԭ������������������Ӳ�����3����DԪ�ص���������ϼ���������ϼ۵ľ���ֵ��ȣ���D��Cֻ���γ�һ�ֻ����E�����ڿ�����ȼ��������һ�ֵ���ɫ���塣�Իش�
(1)AԪ������__________������Ԫ�����ڱ��е�λ��___________ ��BԪ��ԭ�ӵĵ���ʽ___________��EԪ�ؼ����ӵĵ����Ų�ʽ��___________��
(2)�ֱ�д��A��B������������Ӧˮ����ķ���ʽ________��_________
(3)д��C��D�γɵĻ�����Ļ�ѧʽ__________��������ԭ�ӹ�����ӻ���ʽ��___________��
(4)д��A����̬�⻯��Ľṹʽ_________������ӵĿռ乹��Ϊ_________������___________���ӡ�
�ο��𰸣�(1)�����ڶ�����VA�壻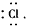 ��1s22s22p6
��1s22s22p6
(2)HNO3��HClO4
(3)SiO2��sp3
(4)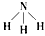 ������������
������������
���������
�����Ѷȣ�һ��
5���ƶ��� W��X��Y��Z�����ڱ�ǰ36��Ԫ���е����ֳ���Ԫ�أ���ԭ��������������W��Y���������ǵ����������Ҫ���ʣ�X�Ļ�̬ԭ�Ӻ�����7��ԭ�ӹ������˵��ӣ�Z���γɺ�ɫ����ש��ɫ���ĺͺ�ɫ��ZO���������
��1��Wλ��Ԫ�����ڱ���_________���ڵ�_________�塣W����̬�⻯���ȶ��Ա� __________���ǿ������������
��2��Y�Ļ�̬ԭ�Ӻ�������Ų�ʽ��________��Y�ĵ�һ�����ܱ�X��__________�����С������
��3��Y������������Ӧˮ�����Ũ��Һ��Z�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽ��_____________________
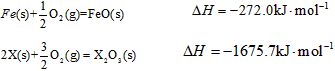
X�ĵ��ʺ�FeO��Ӧ���Ȼ�ѧ����ʽ��______________________________��
�ο��𰸣���1������VA����
��2��1s22s22p63s23p4����
��3��Cu+2H2SO4(Ũ) CuSO4+SO2��+2H2O��3FeO(s)+2Al(s)==Al2O3(s)+3Fe(s) ��H=-859.7kJ/mol
CuSO4+SO2��+2H2O��3FeO(s)+2Al(s)==Al2O3(s)+3Fe(s) ��H=-859.7kJ/mol
���������
�����Ѷȣ�һ��