1��ѡ���� ��֪��ӦN2��g����3H2��g��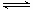 2NH3��g������H��0����ij����㶨���ܱ������а������1:3����N2��H2����һ�������·�����Ӧ����ͼ��ij��������Y����ʱ�䣨t���仯��ʾ��ͼ��ͼ��T��ʾ�¶ȣ���Y������
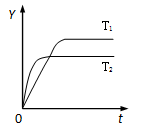
2NH3��g������H��0����ij����㶨���ܱ������а������1:3����N2��H2����һ�������·�����Ӧ����ͼ��ij��������Y����ʱ�䣨t���仯��ʾ��ͼ��ͼ��T��ʾ�¶ȣ���Y������
 ?
?
A��N2��ת����
B�����������ܶ�
C���ܱ�������ѹǿ
D��H2���������
�ο��𰸣�A
�������������ͼ���֪�¶�ΪT2�����ߵ���ƽ���ʱ���٣�˵����Ӧ���ʴ�����T2����T1����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ�����Ӧ���ת���ʽ��ͣ�����������������С���ܶ�������������������ݻ��ı�ֵ���Dz���ġ��¶����ߣ���������ʵ��������ӣ�����ѹǿҪ���������ȷ�Ĵ���A��
�����Ѷȣ�һ��
2������� �����������ܱ������г���2 mol N2��6 mol H2��һ�������·�����Ӧ��
N2������+ 3 H2������ 2 NH3��������ƽ��ʱ�������7 mol����a��b��c�ֱ����N2��H2��NH3��ʼ��������ʵ�����ά���¶Ȳ��䣬ʹ�ﵽƽ��ʱ���ɷֵİٷֺ������䣮��
2 NH3��������ƽ��ʱ�������7 mol����a��b��c�ֱ����N2��H2��NH3��ʼ��������ʵ�����ά���¶Ȳ��䣬ʹ�ﵽƽ��ʱ���ɷֵİٷֺ������䣮��
��1����a��0��b��0����c��? ��
��2����a��0.7��b��2.1����
��c��? ��
����ʱ��Ӧ��?���У�
����Ҫά�ַ�Ӧ��ʼ��÷�Ӧ������У�c�ķ�Χ��? ��
��3����ʹ��ʼ��Ӧά��������෴�ķ�����У���b�ķ�Χ��? ��
�ο��𰸣���1��4
��2��2.6���淴Ӧ����1��C��4��
��3��4.5��b��6
���������
�����Ѷȣ�����
3��ѡ���� �Կ��淴ӦN2 + 3H2 2NH3������������˵����Ӧ�Ѵ�ƽ�����?��?��?
2NH3������������˵����Ӧ�Ѵ�ƽ�����?��?��?
A����λʱ������a mol N2���ģ�ͬʱ����2a mol NH3
B��������Ũ�Ȳ��ٱ仯
C�������ڵ�����������������Ũ��֮��Ϊ1�U3�U2
D����ѧ��Ӧ���ʹ�ϵ�ǣ�2v����NH3�� = 3v�棨H2��
�ο��𰸣�B
�����������
�����Ѷȣ���
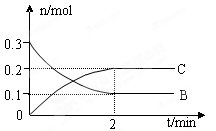
4��ѡ���� һ���¶��£���2L���ܱ������з�����Ӧ��A(g) + 2B(g) xC(g)?��H �� 0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ��ʾ�������й�˵������ȷ����
xC(g)?��H �� 0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ��ʾ�������й�˵������ȷ����
A����=2
B��2min�����¶�ƽ�������ƶ�
C����Ӧ��ʼ2min�ڦ�(C) = 0��1mol/(L��min)
D���������ڻ������ѹǿ���ٸı�ʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬
�ο��𰸣�C
�����������ͼ֪��2min�ڡ�nB=0��2mol����nC=0��2mol�����Է�Ӧ��BC��ϵ������ȵģ���=2����ȷ����ΪA(g) + 2B(g) xC(g)?��H �� 0�������¶�ƽ�������ƶ���B��ȷ��C����Ӧ��ʼ2min�ڦ�(C) = 0��05mol/(L��min)��C�����ں����ܱ�������A(g) + 2B(g)
xC(g)?��H �� 0�������¶�ƽ�������ƶ���B��ȷ��C����Ӧ��ʼ2min�ڦ�(C) = 0��05mol/(L��min)��C�����ں����ܱ�������A(g) + 2B(g) xC(g)?����Vg��0, ���Ե������ڻ������ѹǿ���ٸı�ʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬����ȷ��
xC(g)?����Vg��0, ���Ե������ڻ������ѹǿ���ٸı�ʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬����ȷ��
�����Ѷȣ�һ��
5������� ��һ�������£���һ�ݻ��ɱ���ܱ������У���SO2��O2��Ϸ�����Ӧ��
2SO2(g)��O2(g)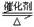 2SO3(g)?��H����92.3KJ/mol����Ӧ�����У�SO2��O2��SO3�����ʵ���(mol)�ı仯���±���0��4minʱ����������ѹǿΪ0.1MPa����
2SO3(g)?��H����92.3KJ/mol����Ӧ�����У�SO2��O2��SO3�����ʵ���(mol)�ı仯���±���0��4minʱ����������ѹǿΪ0.1MPa����
ʱ��min
| 0
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
|
n(SO2)
| 2.00
| 1.92
| 1.84
| 1.76
| 1.76
| 1.64
| 1.52
| 1.40
| 1.40
| 1.40
|
n(O2)
| 1.00
| 0.96
| 0.92
| 0.88
| 0.88
| 0.82
| 0.76
| 0.70
| 0.70
| 0.70
|
n(SO3)
| 0
| 0.08
| 0.16
| 0.24
| 0.24
| 0.36
| 0.48
| 0.60
| 0.60
| 0.60
|
?
�ش��������⣺
��1��___________________________ʱ�Σ���Ӧ����ƽ��״̬��
��2����5minʱ����ͬʱ������ʺ�ת������������������ı�����������_____________��ƽ����____________�����ƶ���������������桱������
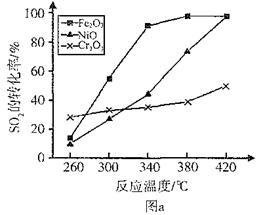
��3������������ͬ��������ͬʱ��SO2��ת�����淴Ӧ�¶ȵı仯��ͼa����Fe2O3��NiO����������ʹS02��ת���ʴﵽ��ߣ������Ǽ۸����أ�ѡ��Fe2O3�� ��Ҫ�ŵ���_____________��
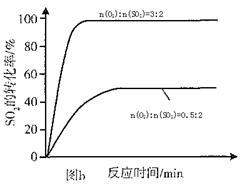
��4������С����3800C Fe2O3������ʱ���о��˲�ͬͶ�ϱ�n(O2):n(SO2)��S02ת���ʵ�Ӱ�죬�����ͼb�����ڴ������ͼ�л���n(O2):n(SO2)=1:2ʱ��SO2ת���ʵ�Ԥ�ڱ仯���ߡ�
�ο��𰸣���1��3��4min(2��)? 7��9min(2��)��2������ѹǿ(2��)����(2��)?
��3��Cr2O3? (2��) Fe2O3������ʱ������Խϵ��¶ȿɻ�ýϸ�SO2��ת���ʡ���2�֣�
��4����3�֣�����ע1�֣�ת�۵�1�֣�ƽ̨1�֣�
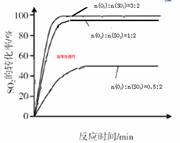
�����������1���ɱ����е����ݷ���֪��3��4min��7��9minʱSO2��O2��SO3�����ʵ������ֲ��䣬Ϊ��ѧƽ��״̬����2���ӱ������ݷ�������5minʱ��SO2��O2�����ʵ�����С��SO3�����ʵ�������˵��ƽ���������ƶ����÷�ӦΪ���ȷ�Ӧ���ı����������Ϊ����ѹǿ���¶ȣ������·�Ӧ���ʱ�������ͬʱ������ʺ�ת������������������ı���������ֻ��������ѹǿ����3����ͼ���֪��������������ͬʱ��2600C��Cr2O3��������SO2��ת�������Ӧ������죻�Աȷֱ���Fe2O3��NiO��������ͼ��֪����Fe2O3������ʱ�����ڽϵ͵��¶���ʹSO2�ﵽ�ϸߵ�ת���ʣ����ѡ��Fe2O3����4������ͼ��b֪����SO2�����ʵ�����ͬʱ��O2�����ʵ���Խ��ƽ���ʱ��Խ�̣���Ӧ����Խ�죬SO2��ƽ��ת����Խ���Դ˿ɻ���n(O2):n(SO2)=1:2ʱSO2ת���ʵ�Ԥ�ڱ仯���ߡ�
�����Ѷȣ�һ��