1、选择题 A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大。已知:B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2。由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y,A与C形成的气态化合物Z在标准状况下的密度为0.76g/L,Z溶于水所得溶液为W。下列说法正确的是
[? ]
A.?元素C在周期表中的位置是第三周期第ⅤA族
B.?在等体积、等pH的X、Y溶液中分别加入等质量的锌粉,充分反应后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X<Y
C.?由A、B、C、D四种元素形成的化合物一定只有共价键
D.?25℃时,将0.1?mol/L的W与0.1?mol/L的Y溶液等体积混合,充分反应后若pH=7 则溶液中?c(CA4+)=c(F-)
2、选择题 25℃时,某氢氧化钠溶液跟醋酸溶液等体积混合后,恰好完全反应,下列关系一定正确的是
[? ]
A.混合前两种溶液pH之和等于14
B.混合前碱溶液跟酸溶液的物质的量浓度相等
C.混合后溶液中c(Na+)=c(CH3COO-)
D.混合后溶液c(Na+)>c(CH3COO-)>c(CH3COOH)>c(OH-)>c(H+)
3、选择题 有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COOK与HCl;②CH3COOK与KOH;③CH3COOK与KCl;④CH3COOK与KHC03下列各项排序正确的是( )
A.c(CH3C00-):②>④>③>①
B.c(CH3COOH):①>④>③>②
C.pH:②>③>①>④
D.溶液中C(H+):①>③>②>④
4、选择题 下列关于电解质溶液的叙述正确的是?
[? ]
A.0.1 mol・L-1 CH3 COOH溶液加水稀释,溶液中c(H+)和c(OH-)都减小
B.0.1 mol・L-1 CH3COOH溶液中加入CH3COONa固体,溶液中c(OH-)减小
C.0.1 mol・L-1 CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+)
D.相同浓度的CH3 COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小
5、填空题 北京奥运会“祥云”火炬燃料是阿烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯已知
C3H8(g)=CH4(g)+HC=CH(g)+H2(g) △H1=156.6 kJ/mol。
CH3CH=CH2(g)=CH4(g)+HC=CH(g) △H2=32.4 kJ/mol。
则相同条件下,反应C3H8(g)=CH3CH=CH2(g) +H2(g)的△H=___________ kJ/mol。
(2)以丙烷为燃料制作的新型燃料电池。电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程程式为__________;放电时,CO32-移向电池的________(填“正”或“负”)极。
(3)碳氢化台物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水.达到平衡时,溶液的pH=
5.60,c(H2CO3)=1.5×10-5 mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3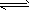 HCO3-+H+的平衡常数K1=__________(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=__________(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)______c(CO32-) (填“>”、“=”或“<”),原因是____________________(用离子方程式和必要的文字说明)。