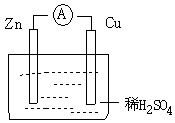
1、选择题 如图所示的原电池装置,下列说法不正确的是
[? ]
A.该装置的能量转化形式为:化学能转化为电能
B.电子由Zn片经过导线流向铜片
C.Zn为负极发生还原反应
D.Cu为正极,在Cu片上有气泡产生
参考答案:C
本题解析:
本题难度:简单
2、填空题 某同学想测定A,B,C3种金属的活动性顺序,他把这3 种金属放到相同物质的量浓度的盐酸中,反应速率都较慢,不易分辨出三者的差异,现只有盐酸1种化学试剂,应该用什么方法迅速测出3种金属的活动性顺序? __________________________________
参考答案:将A,B,C3种金属两两连接起来,放入盐酸溶液中,观察哪种金属上产生气泡,则其活动性就较差。
本题解析:
本题难度:一般
3、填空题 (11分)
Ⅰ.(5分)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀,一段时间后某极产生3.36 L(标准状况)的气体。问:
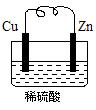
(1)负极是?(填“锌”或“铜”),发生?反应(填“氧?化”或“还原”)。
(2)正极的电极反应为?
(3)产生这些气体共需转移电子?mol。
Ⅱ.(6分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答:

(1)氢氧燃料电池的能量转化主要形式是?,在导线中电子流动方向为 ? (用a、b表示)。
(2)负极反应式为?。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一金属锂是一种重要的储氢材料,吸氢和放氢原理为:?Ⅰ.2Li+H2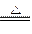 2LiH?Ⅱ.LiH+H2O===LiOH+H2↑
2LiH?Ⅱ.LiH+H2O===LiOH+H2↑
反应Ⅰ中的还原剂是 ? ,反应Ⅱ中的氧化剂是 ? 。
参考答案:(11分)
(Ⅰ)(5分)
(1)锌;氧化(各1分)
(2)2H++2e-=H2↑ (2分)
(3)0.3(1分)
(Ⅱ)(6分)
(1)由化学能转变为电能;?由a到b;(各1分)
(2)2H2+4OH―4e- ===4H2O?或? H2+2OH―2e-===?2H2O(2分)
(3)Li? H2O(各1分)
本题解析:略
本题难度:一般
4、填空题 选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn+CuSO4=ZnSO4+Cu
(1)画出装置图:______
(2)电极材料和电解质溶液各是什么?______
(3)写出电极反应式:
正极:______;负极:______.
参考答案:(1)根据自发的氧化还原反应:金属锌失电子,为负极,正极可以用活泼性较差的金属铜,溶液中的铜离子得电子,必须用可溶的铜盐作电解质,结合原电池的构成条件,装置为:

,故答案为:

;
(2)负极是失去电子的极,金属要比正极活泼,氧化还原反应中金属锌失电子,所以负极为锌片,正极可以是金属铜(或者碳棒),电解质溶液为可溶的铜盐,如氯化铜或硫酸铜等,故答案为:负极:锌片,正极:铜片(或碳棒),电溶解质:CuSO4溶液(或CuCl2溶液);
(3)负极是负极是电极本身发生失电子的氧化反应,即Zn-2e-=Zn2+,正极是电解质中的阳离子发生得电子的还原反应,即Cu2+2e-=Cu,故答案为:Zn-2e-=Zn2+;Cu2+2e-=Cu.
本题解析:
本题难度:一般
5、选择题 将0.1L含有0.02mol?CuSO4和0.01molNaCl的水溶液用惰性电极电解.电解一段时间后,一个电极上得到0.01mol?Cu,另一电极析出的气体( )
A.只有Cl2
B.只有O2
C.既有Cl2又有O2
D.只有H2
参考答案:溶液中含有n(Cu2+)=0.02mol,n(Cl-)=0.01mol;用惰性电极电解,电解一段时间后,一个电极上得到0.01mol Cu,是阴极反应,另一电极析出的气体为阳极反应;发生的电极反应为:根据得到铜物质的量计算电子转移,阳极电子转移守恒分析判断离子反应情况;
阳极电极反应:2Cl--2e-=Cl2↑;
?0.01mol 0.01mol
? 4OH--4e-=2H2O+O2↑
?0.01mol? 0.01mol
阴极电极反应:Cu2++2e-=Cu;
?0.02mol? 0.01mol
依据上述分析和计算得到,阳极反应生成的气体是氧气和氯气;
故选C.
本题解析:
本题难度:一般