1、填空题 (12分)Al及其化合物用途广泛,工业上可以将明矾石经处理后得到明矾[KAl(SO4)2・12H2O],再将明矾焙烧后制得Al2O3等物质,进一步处理后还可以得到Al。
已知焙烧明矾的化学方程式为:
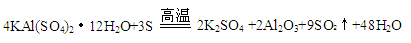
请回答:
(1)Al2O3的摩尔质量是 。
(2)工业上可用电解Al2O3制备Al,其化学方程式是 。
(3)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比是 。
(4)焙烧明矾时产生的SO2可综合利用来制硫酸。
已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1 = 一197 kJ/mol
2SO3(g) △H1 = 一197 kJ/mol
2H2O (g)=2H2O(1) △H2 = 一44 kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3 = 一545 kJ/mol
SO3(g)与H2O(l)反应的热化学方程式是 。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式 。
②电池总反应的化学方程式 。
2、选择题 常温时,用某新型充电电池电解如右图所示的l00mL溶液,充电电池的总反应为
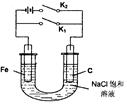
4Li+2SOCl2  ?4LiCl +S+SO2,则下列叙述中不正确的是
?4LiCl +S+SO2,则下列叙述中不正确的是
A.若仅闭合K2,铁极的电极反应式:Fe - 2e=Fe2+
B.放电时电池上正极的电极反应式为:2SOCl2+4e =4C1-+S+SO2
C.若仅闭合K1,电子由Fe极沿导线流向C极
D.若不考虑气体溶解和溶液体积变化,当电池中生成0. 025molS时,溶液中pH=14
3、选择题 如图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑点向d端扩散。下列判断正确的是( )

A.滤纸上c点附近会变红色
B.Cu电极质量减小,Pt电极质量增大
C.Z中溶液的pH先减小,后增大
D.溶液中的SO42―向Cu电极定向移动
4、选择题 以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
A.电能全部转化为化学能
B.粗铜接电源正极,发生还原反应
C.溶液中Cu2+向阳极移动
D.利用阳极泥可回收Ag、Pt、Au等金属
5、简答题 (14分)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol.L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中x值:
(列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为 。在实验室中,FeCl2可用铁粉和 盐酸反应制备,FeCl3可用铁粉和 反应制备;
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为 ,该电池总反应的离子方程式为 。