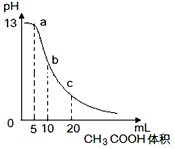
1、选择题 25℃时,向体积为10mL 0.1mol/L NaOH溶液中逐滴加入0.1mol/L的CH3COOH溶液,曲线如图所示,有关离子浓度关系的比较中,错误的是
[ ? ]
A.a点处:c(Na+)> c(CH3COO-)> c(OH-)>c(H+)
B.b点处:c(CH3COOH)+c(H+)=c(OH-)
C.c点处:c(CH3COOH)+ c(CH3COO-)=2c(Na+)
D.NaOH溶液和CH3COOH溶液任意比混合时:c(Na+)+c(H+)=c(OH-)+ c(CH3COO-)
参考答案:A
本题解析:
本题难度:一般
2、选择题 对下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
A.某溶液中存在的离子只有Cl-、OH-、NH4+、H+,该溶液中离子浓度大小关系可能为c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.0.1?mol?L-1(NH4)2SO4溶液中:c(H+)>c(NH4+)
C.0.1?mol?L-1的HCl溶液与0.1?mol?L-1的NaOH溶液等体积混合:c(H+)+c(Na+)=c?(OH-)+c(Cl-)
D.0.1?mol?L-1?CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
参考答案:A.溶液呈电中性,溶液中阴阳离子所带电荷相等,则c(Cl-)+c(OH-)=c(NH4+)+c(H+),如果c(Cl-)>c(NH4+),则c(OH-)<c(H+),故A错误;
B.硫酸铵是强酸弱碱盐,铵根离子易水解,但水解程度较小,所以c(H+)<c(NH4+),故B错误;
C.0.1mol?L-1的HCl溶液与0.1?mol?L-1的NaOH溶液等体积混合,盐酸和氢氧化钠恰好完全反应生成氯化钠,溶液呈电中性,溶液中阴阳离子所带电荷相等,则c(H+)+c(Na+)=c?(OH-)+c(Cl-),故C正确;
D.醋酸钠是强碱弱酸盐,醋酸根离子易水解,钠离子不水解,所以c(Na+)>c(CH3COO-),醋酸根离子水解而使溶液呈碱性,所以c(OH-)>c(H+),醋酸根离子水解较微弱,所以c(CH3COO-)>c(OH-),故D错误;
故选C.
本题解析:
本题难度:简单
3、选择题 在25℃时将pH=11 的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是
[? ]
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(H+)=c(CH3COO-)+c(OH-)
C.c(Na+)>c (CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
参考答案:D
本题解析:
本题难度:一般
4、选择题 相同温度时,有关①100 mL0.1mol/LNaHCO3、②100 mL0.1mol/LNa2CO3两种溶液的叙述不正确的是
[? ]
A. ①溶液中:c(CO32-)<c(H2CO3)
B. 溶液的pH:②>①
C. 溶液中的阴离子种类:②>①
D. ②溶液中:c(HCO3-)>c(H2CO3)
参考答案:C
本题解析:
本题难度:一般
5、选择题 某同学测得物质的量浓度均为0.01mol?L?-1的CH3COOH和CH3COONa的混合溶液呈酸性后,得出下列关系式,你认为其中不正确的是( )
A.c(CH3COO-)>c(CH3COOH)
B.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.c(Na+)=c(CH3COO-)=0.01mol?L-1
D.c(CH3COOH)+c(CH3COO-)=0.02mol?L-1
参考答案:C
本题解析:
本题难度:简单