1、选择题 可用热分解法就可能制得的金属有( ? )
A.CuCr
B.TiW
C.AgHg
D.NaAl
2、实验题 某课外活动小组用如图装置进行实验,试回答下列问题。
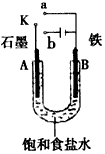
(1)若开始时开关K与a连接,则B极的电极反应式为________________。
(2)若开始时开关K与b连接,则B 极的电极反应式为____________________,总反应的离子方程式为
___________________有关上述实验,下列说法正确的是(填序号)__________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2. 24 L气体,则溶液中转移0.2 mol电子
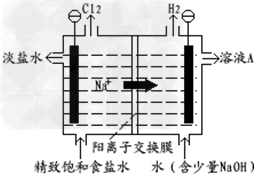
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾 溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为_________________。此时通过阴离子交换膜的离子数_____(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填写“A”、“B”、 “C”或“D”)____导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因_______________________。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为________。
3、填空题 氯碱工业中电解饱和食盐水的原理示意图如图所示:
(1)溶液A的溶质是____________;
(2)电解饱和食盐水的离子方程式是________?;
(3)电解时用盐酸控制阳极区溶液的PH在2~3,用化学平衡移动原理解释盐酸的作用____________?;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42-)>c(Ca2+)]。精致流程如下:
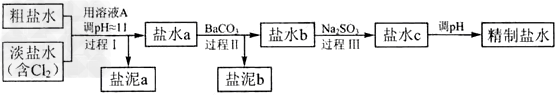
①盐泥a除泥沙外,还含有的物质是_____________。
②过程Ⅰ中将NH4+转化为N2的离子方程式是___________________?
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有_________________?
④经过程Ⅲ处理,要求盐水中c?中剩余Na2SO3的含量小于5mg?/L,若盐水b中NaClO的含量是7.45?mg?/L?,则处理10m3?盐水b?,至多添加10%?Na2SO3溶液_________?kg(溶液体积变化忽略不计)。
4、实验题 某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
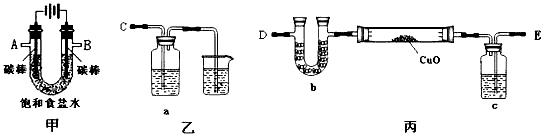
(1)为完成上述实验,正确的连接顺序为_______接A, B接_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为____________________________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液及对应的现象是____________________________。
(4)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案精确测量硬质玻璃管的质量为ag, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为bg,实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为cg,进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量dg,进而确定Cu的相对原子质量。
①请你分析并回答:你认为不合理的方案及其不足之处是_____________________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量______________。
5、选择题 下列关于工业生产的说法,错误的是( )
A.工业上将粗铜进行精炼,应将粗铜连接在电源的正极
B.生产钢化玻璃的主要原料是石灰石、石英和纯碱
C.接触法制硫酸过程中,因为常压下SO2的转化率很高,所以不采用高压
D.合成氨的反应是吸热反应,因此合成氨工业采用高温