1��ѡ���� ����˵����ȷ����
[? ]
A����̼������������������ŷţ�CO2��CH4���dz�������������
B����⾫��ͭʱ����������������3��2gʱ��ת�Ƶĵ�����Ϊ0��1��6��02��1023
C����֪��ӦmX(g)��nY(g)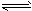 qZ(g) ����ƽ��ʱX��Y��ת������ȣ�˵����Ӧ��ʼʱX��Y�����ʵ���֮��Ϊ1��1
qZ(g) ����ƽ��ʱX��Y��ת������ȣ�˵����Ӧ��ʼʱX��Y�����ʵ���֮��Ϊ1��1
D��C60��Ħ��������720
�ο��𰸣�A
���������
�����Ѷȣ���
2������� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á�һ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺?
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ��?
�ٵ�����X���ϵĵ缫��ӦʽΪ____________________����X�������۲쵽��������_______________��?
��Y�缫�ϵĵ缫��ӦʽΪ___________________,����õ缫��Ӧ����ķ�����__________________��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ?
��X�缫�IJ�����____________________���缫��ӦʽΪ_______________��
��Y�缫�IJ����� ________________���缫��ӦʽΪ___________��?
�ο��𰸣���1����2H++2e-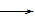 H2���ų����壬��Һ��죻��2Cl--2e-
H2���ų����壬��Һ��죻��2Cl--2e-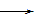 Cl2����ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ
Cl2����ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ
��2���ٴ�ͭ��Cu2++2e-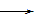 Cu���ڴ�ͭ��Cu-2e-
Cu���ڴ�ͭ��Cu-2e-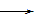 Cu2+?
Cu2+?
���������
�����Ѷȣ�һ��
3������� ����Ͽ�ѧ�ķ�չ�����������仯����õ���Խ��Խ�㷺��Ӧ�ã�Ϊ�������ú�������������V2O5��VOSO4�������Բ�������������Ա����������һ�����ӽ��������շ����¹��գ������ʴ�91.7%���ϣ��ù��յ���Ҫ������ͼ1��
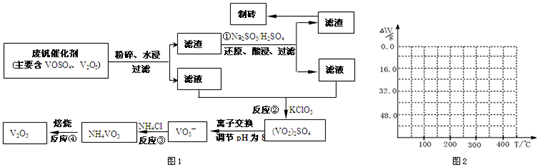
���ַ��Ļ�������ˮ�е��ܽ������±���ʾ���ɴ˻ش��������⣺
| ���� | VOSO4 | V2O5 | NH4VO3 | ��VO2��2SO4
�ܽ���
����
����
����
����
|
��1��23V��Ԫ�����ڱ�λ�ڵ�______����______�壮��ҵ����V2O5ұ���������������ȼ������仯ѧ����ʽΪ______��
��2����Ӧ�ٵ�Ŀ����______��
��3���ⶨ��Ӧ����Һ�з��ĺ�����������֪Ũ�ȵ��ữH2C2O4��Һ�ζ���VO2��2SO4��Һ����Ҫ����ΪCO2��VOSO4�������ӷ���ʽΪ��______��
��4����֪NH4VO3�ڱ��չ�����150��200��ʱ��ʧȥ������300��350����ʧȥˮ�������ұ�����ͼ2�л�������234g?NH4VO3���������ļ���ֵ��W���¶ȣ�T���仯�����ߣ�
�ο��𰸣���1������23V��������������Ϊ23��ԭ�ӣ����Է�Ԫ��λ�ڵ������ڣ���?VB?���壻������ȷ�Ӧ��ԭ��д����ѧ����ʽ���ʴ𰸣��ģ�VB��?3V2O5+10A?����?.?l6V+5Al2O3��
��2������������������ƣ�Ŀ��������������ԭ��Ӧ�����������ƻ�ԭV2O5����V2O5?ת��Ϊ�����Ե�VOSO4�������ᴿ���ʴ𰸣���V2O5?ת��Ϊ�����Ե�VOSO4��
��3���ⶨ��Ӧ����Һ�з��ĺ�����������֪Ũ�ȵ��ữH2C2O4��Һ�ζ���VO2��2SO4��Һ����Ҫ����ΪCO2��VOSO4�����ݻ��ϼ�������д�����ӷ���Ϊ2VO2++H2C2O4+2H+=2?VO2++2?CO2��+2?H2O��
�ʴ𰸣�2VO2++H2C2O4+2H+=2?VO2++2?CO2��+2?H2O��
��4����ʽΪ��
2NH4VO3�TV2O5+2NH3��+H2O
234g?34g?18g
����ֵ��ʼΪ0��34g�����ߴ�150�濪ʼ���٣�34gNH3������200��ʱ����32.0g�����������߿�ʼƽֱ����300��ʱ�ֿ�ʼ���٣�H2O������������350��ʱ����52gʱ����48.0g�Եͣ��Ͳ��ٱ仯������ͼ������

�ʴ�Ϊ��

���������
�����Ѷȣ�һ��
4��ѡ���� �������ʵ��Ʊ������Ϲ�ҵ����ʵ�ʵ��ǣ�������
A����ϴ�Ӽ�������������У������̼ԭ�ӵĸ�����12��18Ϊ��
B���������֣�Ŀ�����ʵ����������еĺ�̼������ȥ����������
C����ˮ��þ��ͨ���������״̬������þ���Ʊ�����þ
D���백��Ƚϣ������Ƽ�ŵ��������ԭ�ϵ�ԭ��������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ұ��K��Ca��Na��Al�Ȼ��ý���ͨ�����õķ����ǣ�������
A���ȷֽⷨ
B���Ȼ�ԭ��
C������������������
D��������ε�ˮ��Һ
�ο��𰸣�C
���������
�����Ѷȣ���