1��ѡ���� ��һ���¶�������̶����ܱ������У����������������ٻ�������ѹǿ?������������ʵ���?�ۻ��������ܶȢ�B�����ʵ���Ũ�Ȳ��ٱ仯ʱ���ܱ������淴ӦA��s��+2B��g��?C��g��+D��g���Ѵ�ƽ����ǣ�������
A���٢�
B���ۢ�
C���٢�
D��ֻ�Т�
�ο��𰸣��ٷ�Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ��������۷�Ӧ�Ƿ�ﵽƽ��״̬����������ѹǿʼ�ղ��䣬�ʢٴ���
�ڷ�Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ��������۷�Ӧ�Ƿ�ﵽƽ��״̬������������ʵ���ʼ�ղ��䣬�ʢڴ���
����A�ǹ��壬��Ӧǰ����������������仯��������������䣬���ﵽƽ��״̬ʱ�����������ܶȲ��䣬�ʢ���ȷ��
�ܵ���Ӧ�ﵽƽ��״̬ʱ��B�����ʵ���Ũ�Ȳ��٣��ʢ���ȷ��
��ѡ��B��
���������
�����Ѷȣ�һ��
2������� �������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��
��1����֪��N2(g)+ O2(g)="2NO(g)" ��H=��180.5 kJ/mol?
2C(s)+ O2(g)="2CO(g)" ��H="-221.0" kJ/mol
C(s)+ O2(g)=CO2(g) ��H="-393.5" kJ/mol
β��ת���ķ�Ӧ֮һ��2NO(g)+2CO(g)=N2(g)+2CO2(g)?��H��?��
��2��ij�о���ѧϰС���ڼ�����Ա��ָ���£���ij�¶�ʱ������������̽��ij�ִ��������µķ�Ӧ���ʣ������崫������ò�ͬʱ���NO��COŨ�������

��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��)��
��ǰ2s�ڵ�ƽ����Ӧ����v (N2) = ___________________��
���ڸ��¶��£���Ӧ��ƽ�ⳣ��K =?����ֻд����������
�۶��ڸÿ��淴Ӧ��ͨ���ۺϷ���������Ϣ�����ٿ���˵��?������ĸ����
A���÷�Ӧ�ķ�Ӧ���Ϻ�ܲ��ȶ�
B���÷�Ӧһ���������ں̵ܶ�ʱ�������
C���÷�Ӧ��ϵ�ﵽƽ��ʱ������һ�ַ�Ӧ��İٷֺ�����С
D���÷�Ӧ��һ�����������Է�����
E���÷�Ӧʹ�ô������岻��
��3��CO��������ȼ�ϵ��Ϊ����ԭ������װ����ͼ��ʾ���õ���е����Ϊ�����ƣ������ƣ�����O2-�����ڹ������NASICON�������ƶ�������˵���������?��
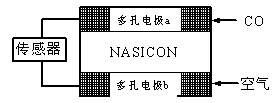
A�������ĵ缫��ӦʽΪ��CO+O2���D2e-��CO2
B������ʱ�缫b��������O2-�ɵ缫a����缫b
C������ʱ�����ɵ缫aͨ������������缫b
D����������ͨ���ĵ���Խ��β����CO�ĺ���Խ��
�ο��𰸣���1��-746.5 kJ/mol(2)��1.88��10��4 mol/(L��s) 5000?��BCD?��3��B
�����������
�����Ѷȣ���
3������� ��12�֣���̼����������Ļ�ѧ����ѧ������ѧ�о����������������û�ʯȼ�ϣ�����̼������Ի����ĸ���Ӱ�졣��ش��������⣺
��1�� 25��ʱ��ʯī��CO��ȼ���ȷֱ�Ϊ��393.5kJ/mol��283.0kJ/mol����д��ʯī����ȫȼ��ʱ���Ȼ�ѧ����ʽ??��
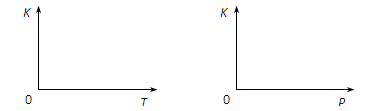
��2��25��ʱ����Ӧ2CO2 (g) 2CO(g)��O2(g)��ƽ�ⳣ��K��2.96��10��92����һ������ɱ���ܱ���������ʼʱ���������Ϊ1L���г���һ������CO2��CO��O2������壬Ҫʹ�����еķ�Ӧ��ʼʱ��CO2�ֽ�ķ����ƶ�������ʼʱ�����������������ʵ���Ӧ����Ĺ�ϵ��?�����÷�Ӧ��25��ʱ�ﵽƽ���������������ʱ�������¶Ȼ�����������ѹǿ������ʹ��ƽ�ⷢ���ƶ����������������������÷�Ӧ��ƽ�ⳣ��K���¶ȣ�T����ѹǿ��P���仯���仯��ʾ��ͼ��
2CO(g)��O2(g)��ƽ�ⳣ��K��2.96��10��92����һ������ɱ���ܱ���������ʼʱ���������Ϊ1L���г���һ������CO2��CO��O2������壬Ҫʹ�����еķ�Ӧ��ʼʱ��CO2�ֽ�ķ����ƶ�������ʼʱ�����������������ʵ���Ӧ����Ĺ�ϵ��?�����÷�Ӧ��25��ʱ�ﵽƽ���������������ʱ�������¶Ȼ�����������ѹǿ������ʹ��ƽ�ⷢ���ƶ����������������������÷�Ӧ��ƽ�ⳣ��K���¶ȣ�T����ѹǿ��P���仯���仯��ʾ��ͼ��
��3�� 1?600��ʱ����Ӧ2CO(g)��O2(g)  2CO2(g)��ƽ�ⳣ��K��1��108�����ⶨ������β����CO��CO2�����Ũ�ȷֱ�Ϊ4.0��10��5mol/L��4.0��10��4mol/L������������������������һ��1?600��IJ�ȼ�������ϲ���O2ʹ��Ũ��ʼ�ձ���Ϊ4.0��10��4mol/L����CO�IJ�ȼת����Ϊ?��
2CO2(g)��ƽ�ⳣ��K��1��108�����ⶨ������β����CO��CO2�����Ũ�ȷֱ�Ϊ4.0��10��5mol/L��4.0��10��4mol/L������������������������һ��1?600��IJ�ȼ�������ϲ���O2ʹ��Ũ��ʼ�ձ���Ϊ4.0��10��4mol/L����CO�IJ�ȼת����Ϊ?��
��4����CO��O2Ϊ�缫ȼ�ϣ�������K2CO3Ϊ��������ȼ�ϵ�أ���д���õ�صĸ�����Ӧ����ʽ?��
�ο��𰸣���1��C��ʯī��+1/2O2��g��==CO(g)?��H="��110.5kJ/mol(" 2�֣�
(2)[ c2(CO)��c(O2)] / c2(CO2)< 2.96��10��92? ( 2�֣�
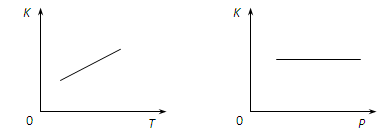
(ÿͼ2�֣�ֻҪ����ʾ��ͼ��ȷ����)
(3)94.5% ��0.5%( 2�֣�? (4)CO-2e-+CO32-=2CO2( 2�֣�
���������д�Ȼ�ѧ����ʽʱҪ����״̬���¶Ȳ���ƽ�ⳣ�����䡣CO-2e-+CO32-=2CO21?600��ʱ����Ӧ2CO(g)��O2(g)  2CO2(g)��ƽ�ⳣ��K��1��108�����ⶨ������β����CO��CO2�����Ũ�ȷֱ�Ϊ4.0��10��5mol/L��4.0��10��4mol/L��
2CO2(g)��ƽ�ⳣ��K��1��108�����ⶨ������β����CO��CO2�����Ũ�ȷֱ�Ϊ4.0��10��5mol/L��4.0��10��4mol/L��
�����Ѷȣ�һ��
4��ѡ���� ���ݻ�һ�����ܱ������У����п��淴ӦN2(g)+3H2(g) 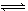 2NH3(g)? ��H��0����ͼ����ʾ�ķ�Ӧ���ߣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾNH3�����������������˵���в���ȷ����
2NH3(g)? ��H��0����ͼ����ʾ�ķ�Ӧ���ߣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾNH3�����������������˵���в���ȷ����
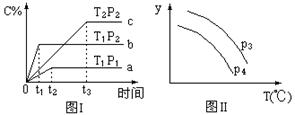
A��T2��T1
B��P2��P1
C����P3��P4��y���ʾN2��ת����
D����P3��P4��y���ʾNH3���������
�ο��𰸣�C
���������A������ͼ1��֪����ѹǿ��ΪP2�������£��¶�ΪT1���������ȴﵽƽ��״̬����˵���¶�ΪT1ʱ��Ӧ���ʿ죬�ﵽƽ���ʱ���١��¶ȸ߷�Ӧ���ʿ죬�����¶���T2��T1��A��ȷ��B��̼������ͼ1��֪�����¶Ⱦ�T1�������£�ѹǿΪP2�����ȴﵽƽ��״̬����˵��ѹǿΪP2ʱ��Ӧ���ʿ죬�ﵽƽ���ʱ���١�ѹǿ��Ӧ���ʿ죬����ѹǿ��P2��P1��B��ȷ��C���÷�Ӧ�������С�Ŀ��淴Ӧ������ѹǿ��Ӧ���ת����������P3��P4����ѹǿΪP4ʱ��ת���ʴ���ѹǿP3ʱ��ת���ʣ�C����ȷ��D������ѹǿƽ��������Ӧ�����ƶ��������������������������P3��P4��y����Ա�ʾNH3�����������D��ȷ����ѡC��
�����Ѷȣ���
5��ʵ���� ��9�֣�ijͬѧ̽��ͬ����Ԫ�����ʵĵݱ���ɣ�������Ӱ�컯ѧ��Ӧ���ʵ����أ�ѡ�õ��Լ����£�þ�������������ۡ��ơ����Ƶ�Na2S��Һ�����Ƶ���ˮ��0.5mol/L�����ᡢ3mol/L�����ᡢ��̪��Һ������Ƶ�ʵ�鷽��������ʵ���������±���
ʵ�鲽��
| ʵ������
|
�ٽ�һС������Ʒ�����з�̪��Һ����ˮ��
| �ƿ鸡��ˮ���ϣ��ۻ���������С�����������ƶ�����֮��ʧ����Һ���ɫ
|
�ڽ������������ͬ��þ����������������ɰֽ��ĥ�����ֱ�Ͷ����������ͬ�����0.5mol/L��������
| þ�����ҷ�Ӧ��Ѹ�ٲ�����������ɫ���壬��������Ӧ��ʮ�־��ң�������ɫ���壬þ����ʧ��������
|
�۽����Ƶ���ˮ�μӵ����Ƶ�Na2S��Һ��
| ?
|
�ܽ���ͬ������þ��������ɰֽ��ĥ���������۷ֱ�Ͷ�뵽��������ͬ�����0.5mol/L�������3mol/L��������
| ���ҷ�Ӧ�������壬��������ʧ��þ����
|
?
��ش��������⣺
��1��ʵ��۵�������?���÷�Ӧ�����ӷ���ʽΪ?��
��2����ʵ��۵ó���ʵ�������?
��3����ʵ��ڿɵó�������ѧ��Ӧ��������Ҫ������?
��4��ʵ����У���Ϊ������ʧ���õ�ʱ��̣���ˣ���ͬѧ�ó����ۣ�����þ��ʧ���ӣ��ý����Ƿ���ȷ��??�����ǻ��
��5��ͨ��ʵ���˵��Ҫ�ӿ컯ѧ��Ӧ���ʿ�?��?��
�ο��𰸣���1�����ɻ�ɫ����? Cl2 + S2�� = 2Cl��+ S����2�֣�
��2����ԭ�ӵõ�������ǿ����ԭ�ӵõ�������������������ͬ���÷֣���2�֣�
��3����Ӧ�ﱾ��������
��4����
��5������Ӧ��Ũ��?����Ӧ��Ӵ�����������ע�������⣬ÿ��1�֣�
�����������
�����Ѷȣ���