1、选择题 下列离子方程式正确的是 (?)
A.NH4HCO3溶液与过量NaOH溶液反应:NH 4++ OH―=NH3↑+ H2O
B.用惰性电极电解饱和氯化钠溶液:2Cl― + 2H +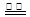 H2↑+ Cl2↑
H2↑+ Cl2↑
C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I―= 2Fe2++I2
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32― + 6H+ + 2MnO4―=5SO42― + 2Mn2+ +3H2O
参考答案:D
本题解析:A.NH4HCO3溶液与过量NaOH溶液反应:NH 4++ HCO3-+ 2OH―=NH3·H2O +H2O+ CO32-
错误。B.用惰性电极电解饱和氯化钠溶液:2Cl― + 2H2O H2↑+ Cl2↑+2OH-。错误。C.向Fe(NO3)溶液中加入过量的HI溶液:8H++2NO3-+6I―=2NO↑+3I2+4H2O.错误。D.符合客观事实。符合电子守恒和原子守恒和电荷守恒。正确。
H2↑+ Cl2↑+2OH-。错误。C.向Fe(NO3)溶液中加入过量的HI溶液:8H++2NO3-+6I―=2NO↑+3I2+4H2O.错误。D.符合客观事实。符合电子守恒和原子守恒和电荷守恒。正确。
本题难度:一般
2、选择题 下列有关方程式书写正确的是( )
A.NaHCO3的电离:NaHCO3 Na++H++C
Na++H++C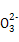
B.HS-的水解:HS-+H2O H3O++S2-
H3O++S2-
C.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e- 4OH-
4OH-
D.用饱和Na2CO3溶液处理重晶石:BaSO4+C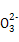
 BaCO3+S
BaCO3+S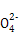
参考答案:D
本题解析:碳酸氢钠是强电解质,应该是NaHCO3 Na++HC
Na++HC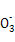 ,A不正确;所给方程式是电离方程式,水解方程式是HS-+H2O
,A不正确;所给方程式是电离方程式,水解方程式是HS-+H2O H2S+OH-,B不正确;氢氧燃料电池中负极是失去电子的,所以氧气在正极通入,C不正确。
H2S+OH-,B不正确;氢氧燃料电池中负极是失去电子的,所以氧气在正极通入,C不正确。
本题难度:一般
3、选择题 下列反应的离子方程式书写正确的是:
A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN- = Fe(SCN)3↓
B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2= I2 + 2H2O
C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH- = Na2SiO3↓+H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3- + OH-+ Ba2+ = H2O + BaCO3↓
参考答案:B
本题解析:A、Fe3+与SCN- 反应生成的Fe(SCN)3不是沉淀,而是一种络合物,A不正确;
B、双氧水具有强氧化性,能把碘离子氧化生成单质碘,而双氧水的还原产物是水,B正确;
C、硅酸钠是可溶性强电解质,应该用离子符号表示,C不正确;
D、氢氧化钡不足,因此生成物是碳酸钡沉淀、碳酸钠和水,D不正确,答案选B。
本题难度:简单
4、简答题 现有100mLAlCl3与MgSO4的混合溶液,分成两等份.
(1)向其中一份中加入10mL4mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是______.继续加入lmol/LNaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是______,剩余的沉淀的物质的量是______.
(2)向另一份中加入amL0.1mol/LBaCl2溶液能使SO42-沉淀完全,a=______.
参考答案:(1)向其中一份中加入10mL 4mol/L的氨水,恰好完全反应反应为A13++3NH3?H2O=Al(OH)3↓+3NH4+;Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+;继续加入l mol/L NaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是Al(OH)3+OH-=[Al(OH)4]-,计算得到氢氧化铝物质的量为0.01mol,消耗一水合氨物质的量0.03mol,所以沉淀镁离子的一水合氨物质的量为0.01mol,镁离子物质的量为0.005mol,生成氢氧化镁沉淀物质的量为0.005mol;
故答案为:A13++3NH3?H2O=Al(OH)3↓+3NH4+;Al(OH)3+OH-=[Al(OH)4]-;0.005mol;
(2)依据(1)计算得到镁离子物质的量为0.005mol,原混合溶液中含有硫酸根离子物质的量为0.005mol,依据Ba2++SO42-=BaSO4↓计算得到a1000L×0.1mol/L=0.005mol,a=50;
故答案 为:50.
本题解析:
本题难度:一般
5、选择题 下列离子方程式中正确的是
[? ]
A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH =7 Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
C.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应CH3OH+H2O-6e-=CO2↑+6H+
D.NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
参考答案:B
本题解析:
本题难度:一般