1��ѡ���� ����˵����ȷ����
A��������ؿ��������������
B�������Ҵ������ᶼ���Է���ȡ����Ӧ
C�����顢�Ҵ������ᶼ�������Ʒ�Ӧ��������
D����ά�غ͵�����ˮ��������������
�ο��𰸣�B
���������A ��������鶼���������ط�Ӧ��
B ��ȷ��
C �������鲻�������Ʒ�Ӧ��������
D ��������ˮ������ǰ����ᡣ
�����Ѷȣ�һ��
2������� У�쳧Ư�׳�����22.4L����״����SO2����ѧС��ͬѧ���ݻ�ѧ����ʽZn+2H2SO4��Ũ��
ZnSO4+SO2��+2H2O�����ȡ65.0gп����98%��ŨH2SO4����=1.84g/cm3��110mL��ַ�Ӧ��пȫ���ܽ�����ռ��������������������䣬���Ͼ��ʼ�Ƽ�����������������⣬�����漴���˻أ�
��1����ѧС�����Ƶõ������л��е���Ҫ�������������______�������ʽ�����������ֽ������Ҫԭ����______��
��2��Ϊ֤ʵ��ط�������ѧС���ͬѧ���������ʵ�飬���˻����壨X��ȡ����������̽���������������չ��̣���Ϊȫ���գ���
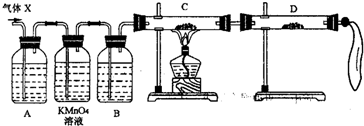
����װ��������ʢ��ҩƷǰ����Ҫ��һ��������______��
��A�м�����Լ������ǣ�______�������ǣ�______��B�м�����Լ������ǣ�______�������ǣ�______��
�ۿ�֤ʵ����X�л��н϶���ij���������ʵ��������______��
��3��������װ���ԼӸĽ����ɴ��ԲⶨX������SO2������������Ľ�ʱ��ѡ�õ���������Ϊ______������ţ���
A?����?B?ˮ��?C?���ƿ?D?����ƿ?E?��Ͳ?F?������?G?˫������
�ο��𰸣���1�����ŷ�Ӧ�Ľ��У�����Ũ�Ƚ��ͣ�п��ϡ���ᷴӦ��������п��H2����ӦΪ��Zn+H2SO4�TZnSO4+H2����
��˻�ѧС�����Ƶõ������л��е���Ҫ��������������������ʴ�Ϊ��H2��
��2����̽���˻����壨X���ijɷ֣�һ��©������̽�����ʴ�Ϊ�����װ�������ԣ�
�����������Ư��ԭ�����������л�ɫ�ؽ�ϳ���ɫ�IJ��ȶ����������A�м�����Լ�������Ʒ����Һ��������ȷ��SO2���ڣ�Ũ���������ˮ�ԣ���ˮ�����и������ã���ֹ���ӵ�ˮ��װ��D�е�����������ţ�
�ʴ�Ϊ��Ʒ����Һ��ȷ��SO2���ڣ�?ŨH2SO4������������
�۸�����Ŀ������װ��ͼ�ͷ�Ӧԭ��֪��װ������ص�װ���Ǽ�����������Ƿ������װ�ã�B��Ũ���ᣬ��ˮ�������ã�C���û�ԭ�����廹ԭ����ͭ��װ�ã�D��ʢ�ŵ�����ˮ����ͭ�������Ƿ���ˮ���ɣ�ֻҪ��ɫ���ɫ����ˮ����ͭ����ɫ����֤�����������ʴ�Ϊ����ɫCuO��ĩ���ɫ����ˮ����ͭ����ɫ��
��3��������Ŀ������װ��ͼ�ͷ�Ӧԭ��֪������C��ֻ������������������ˮ������ˮ���ռ�������Ӧ���ǴӶ̹ܽ����ܳ����ų�ˮ�������������������ʴ�Ϊ��CEG��
���������
�����Ѷȣ���
3��ѡ���� ������ʽΪCxHyOz���л���1mol��O2��ȫȼ�գ�����CO2��ˮ�����������ȣ�����O2 3.5mol������л�����x��y��ֵ�ֱ�Ϊ
A��1��2
B��2��4
C��3��6
D��4��8
�ο��𰸣�C��D
��������������⣬y=2x�����Ը��л������ʽ��дΪ��CxH2xOz�����У�x+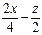 =3.5����֮
=3.5����֮
�����Ѷȣ���
4��ѡ���� ������ʵ��Ũ������ֳ�������(������)��Ӧ��ϵ��ȷ����
[? ]
A���ڿ����г��ھ��õ�Ũ���ᣬ��Һ���������ѻӷ��ԣ�
B���ڼ���������ͭ��Ũ���ᷴӦ��ǿ�����ԡ����ԣ�
C��������Ũ���ᷴӦ���к���״��̿���ɣ���ˮ�ԣ�
D��Ũ�������������ijЩ���壨��ˮ�ԣ�
�ο��𰸣�B
���������
�����Ѷȣ���
5������� A��һ����λ��ȡ��������Է�������Ϊ180�������ԡ�Aˮ������B��C�������Ի����B����Է�������Ϊ60��C������NaHCO3��Һ������ʹFeCl3��Һ��ɫ�������Դ�С�����̼��ӣ�ˮ����д��A��B��C�Ľṹ��ʽ��
A._______________��B.________________��C.________________��
�ο��𰸣�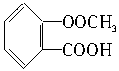 ��CH3COOH��
��CH3COOH��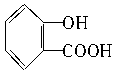
�������������A��ˮ�⣬����A��������ˮ��������������Ի������һ�������ᣬ��һ�����ʾ������ֹ����ţ����������Ƿ��ǻ���ʹFeCl3��Һ��ɫ���͡�COOH������NaHCO3��������B����Է�������Ϊ60�������ᣬC����Է�������Ϊ180+18-60=138���ɴ˿�ȷ��C�Ľṹ��ʽ��
�����Ѷȣ���